-薬物動態-
血中濃度
(1)健康成人への単回投与1)
健康成人男子各12例にそれぞれ、フルティフォーム®50エアゾール1回2吸入(フルチカゾンプロピオン酸エステル100μg/ホルモテロールフマル酸塩水和物10μg)又はフルティフォーム®125エアゾール1回4吸入(フルチカゾンプロピオン酸エステル500μg/ホルモテロールフマル酸塩水和物20μg)を1日2回、7日間投与したときの初回投与後のフルチカゾンプロピオン酸エステル及びホルモテロールの最高血漿中濃度(Cmax)は、フルティフォーム®50エアゾールでそれぞれ21.3±5.68と8.43±4.13、フルティフォーム®125エアゾールでそれぞれ70.9±19.5と26.3±15.9であった。
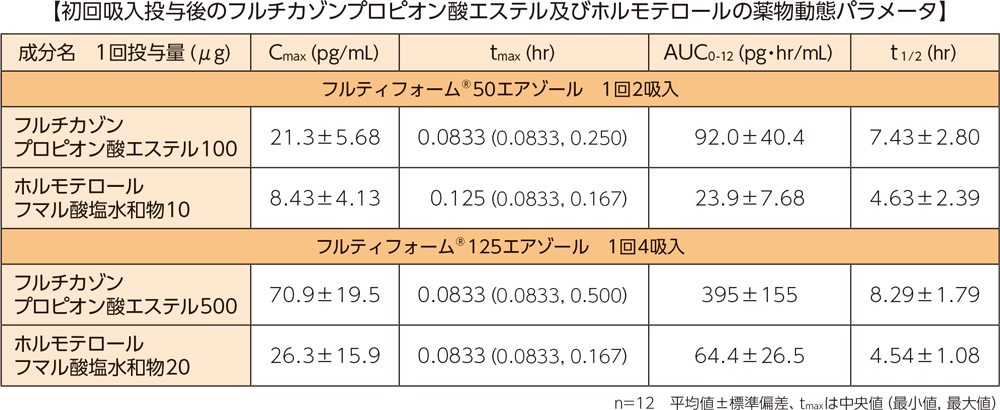
(2)健康成人への反復投与1)
健康成人男子各12例にそれぞれ、フルティフォーム®50エアゾール1回2吸入(フルチカゾンプロピオン酸エステル100μg/ホルモテロールフマル酸塩水和物10μg)又はフルティフォーム®125エアゾール1回4吸入(フルチカゾンプロピオン酸エステル500μg/ホルモテロールフマル酸塩水和物20μg)を1日2回、7日間反復投与したとき、フルチカゾンプロピオン酸エステル及びホルモテロールのCmax及びAUC0-12は、投与7日目には定常状態に達していると考えられ、単回投与に比べ、いずれの用量も2~3倍であった。
7日間反復投与後のフルチカゾンプロピオン酸エステル及びホルモテロールのCmax及びAUC0-12は投与量に比例して増加し、また、半減期はそれぞれ約15時間及び約10時間であった。
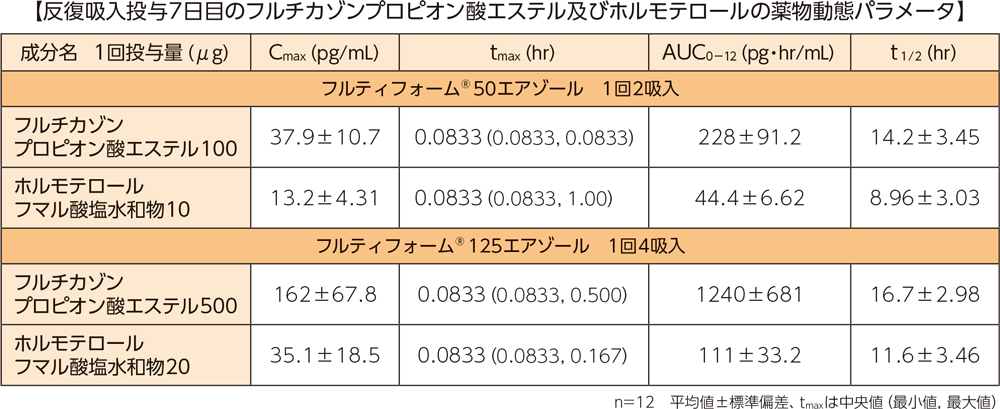
(3)健康成人への反復投与-トラフ血漿中濃度1)
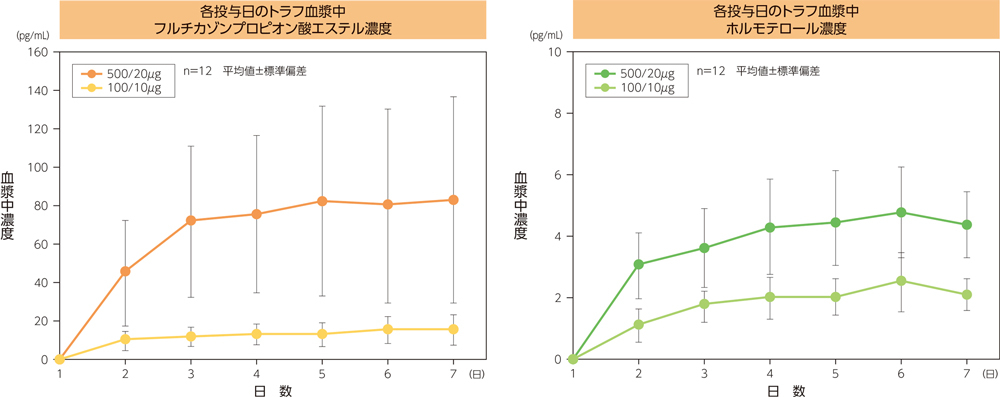
トラフ血漿中フルチカゾンプロピオン酸エステル濃度推移及びトラフ血漿中ホルモテロール濃度推移は以下の通りである。これらの濃度推移より、反復投与7日目までには定常状態に達していると考えられた。
よって、フルチカゾンプロピオン酸エステル及びホルモテロールのCmax及びAUC0-12も、投与7日目には定常状態に達していると考えられ、単回投与に比べ、いずれの用量も2~3倍であった。
6.用法及び用量
-
成人
通常、成人には、フルティフォーム®50エアゾール(フルチカゾンプロピオン酸エステルとして50μg及びホルモテロールフマル酸塩水和物として5μg)を1回2吸入、1日2回投与する。
なお、症状に応じてフルティフォーム®125エアゾール(フルチカゾンプロピオン酸エステルとして125μg及びホルモテロールフマル酸塩水和物として5μg)を1回2~4吸入、1日2回投与する。 -
小児
通常、小児には、フルティフォーム®50エアゾール(フルチカゾンプロピオン酸エステルとして50μg及びホルモテロールフマル酸塩水和物として5μg)を1回2吸入、1日2回投与する。
分布
(1)組織内濃度(ラット)2)
ホルモテロールフマル酸塩水和物
ラットに3H標識ホルモテロール15μg/bodyを気道内噴霧投与したとき、血漿中放射能濃度は投与後5分に最高濃度に達し、その後消失した。投与部位である肺及び気管には高い放射能濃度が認められた。次いで腎臓、血管、食道、心臓、甲状腺及び副腎で高い放射能が認められた。また、放射能は体内に広く分布したが、大脳、小脳、延髄では低かった。投与後5分から4時間までに、すべての組織で最高放射能濃度に達したのち血漿中放射能濃度推移と平行して組織中放射能濃度は消失した。
(2)蛋白結合率(in vitro)3)、4)
ヒト血漿中におけるフルチカゾンプロピオン酸エステル及びホルモテロールの蛋白結合率は、それぞれ81~95%3)及び61~64%4)であった。
代謝・排泄〈外国人データ〉
フルチカゾンプロピオン酸エステル5)
代謝部位:肝臓
健康成人被験者に3H標識フルチカゾンプロピオン酸エステルを1mg又は16mg経口投与したとき、投与後168時間までの尿中に投与放射能の1~5%が排泄されたが、未変化体は検出されず、17β-カルボン酸体及びグルクロン酸抱合体が認められた。糞中には投与放射能の約90%以上が排泄され、未変化体及び主代謝物として17β-カルボン酸体が認められた。
ホルモテロールフマル酸塩水和物6)
代謝部位:肝臓
健康成人被験者に3H標識ホルモテロール37μgを経口投与後直ちに3H標識ホルモテロール16μgを静脈内持続注入(30分)したとき、投与後168時間までに投与放射能の62%が尿中に、24%が糞中に排泄された。この時の血漿及び尿中の主代謝物はホルモテロールのグルクロン酸抱合体であり、尿中にはO-脱メチル化体のグルクロン酸抱合体も認められた。
代謝酵素(in vitro)
フルチカゾンプロピオン酸エステル7)
主として肝チトクロームP-450 3A4(CYP3A4)で主代謝物である17β-カルボン酸体に代謝される。
ホルモテロールフマル酸塩水和物4)
主としてグルクロン酸抱合を受ける。また、ホルモテロールのO-脱メチル化には、CYP2D6、CYP2C19、CYP2C9及びCYP2A6が関与する。
10.相互作用
フルチカゾンプロピオン酸エステルは、主として肝チトクロームP-450 3A4(CYP3A4)で代謝される。
10.1 併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|
デスモプレシン酢酸塩水和物 ミニリンメルト(男性における夜間多尿による夜間頻尿) |
低ナトリウム血症が発現するおそれがある。 | 機序不明。 |
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|
CYP3A4阻害作用を有する薬剤 リトナビル等 |
副腎皮質ステロイド剤を全身投与した場合と同様の症状があらわれる可能性がある。 特に、リトナビルとフルチカゾンプロピオン酸エステル製剤の併用により、クッシング症候群、副腎皮質機能抑制等が報告されている。 |
CYP3A4による代謝が阻害されることにより、フルチカゾンプロピオン酸エステルの血中濃度が上昇する可能性がある。 |
|
カテコールアミン
アドレナリン |
不整脈、場合によっては心停止を起こすおそれがあるので、副作用の発現に注意し、異常が認められた場合には減量又は投与を中止するなど適切な処置を行うこと。 | 併用により、アドレナリン作動性神経刺激の増大が起きる。そのため、不整脈を起こすことがある。 |
|
キサンチン誘導体
テオフィリン |
低カリウム血症による不整脈を起こすおそれがある。血清カリウム値のモニターを行うことが望ましい。 | キサンチン誘導体はアドレナリン作動性神経刺激を増大させるため、血清カリウム値の低下を増強することがある。 |
|
ステロイド剤
プレドニゾロン |
ステロイド剤及び利尿剤は尿細管でのカリウム排泄促進作用があるため、血清カリウム値の低下が増強することが考えられる。 | |
|
利尿剤 フロセミド等 |
||
|
β遮断剤 アテノロール等 |
ホルモテロールの作用を減弱する可能性がある。 | β受容体において競合的に拮抗する。 |
|
QT間隔延長を起こすことが知られている薬剤
抗不整脈剤 |
QT間隔が延長され心室性不整脈等のリスクが増大するおそれがある。 | いずれもQT間隔を延長させる可能性がある。 |
- 1)フルティフォーム®の第Ⅰ相臨床薬理試験(社内資料).
- 2)フルティフォーム®の組織内濃度(社内資料).
- 3)Daniel MJ 他. 基礎と臨床 26;2011, 1992.
- 4)Cheer SM et al. Am J Respir Med 1;285, 2002.
- 5)Harding SM. Respir Med 84;Suppl A, 25, 1990.
- 6)Rosenborg J et al. Drug Metab Dispos 27;1104, 1999.
- 7)Pearce RE et al. Drug Metab Dispos 34;1035, 2006.
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

