-薬効薬理-
腸内細菌叢に対する影響1)
日本人健康成人男性6例にラスクフロキサシン400mgを1日1回7日間反復経口投与し、腸内細菌叢に対する影響を検討した。その結果、健康成人6例中2例の糞便検体において、総菌数が1/10以下に低下したが、投与終了後3週間までに、いずれの菌種でも投与前の菌数にほぼ回復した。その他の患者では、反復投与期間中及び反復投与期間後に総菌数の大きな変動は認められなかった。一方、6例中4例以上において、検査対象とした多くの菌種で菌数の減少が認められた。
また、1例は投与終了後3週間にC. difficileが検出され、C. difficile Toxinは陽性であった。
通常、成人には、ラスクフロキサシンとして1回75mgを1日1回経口投与する。
QT/QTc間隔延長に対する作用1)
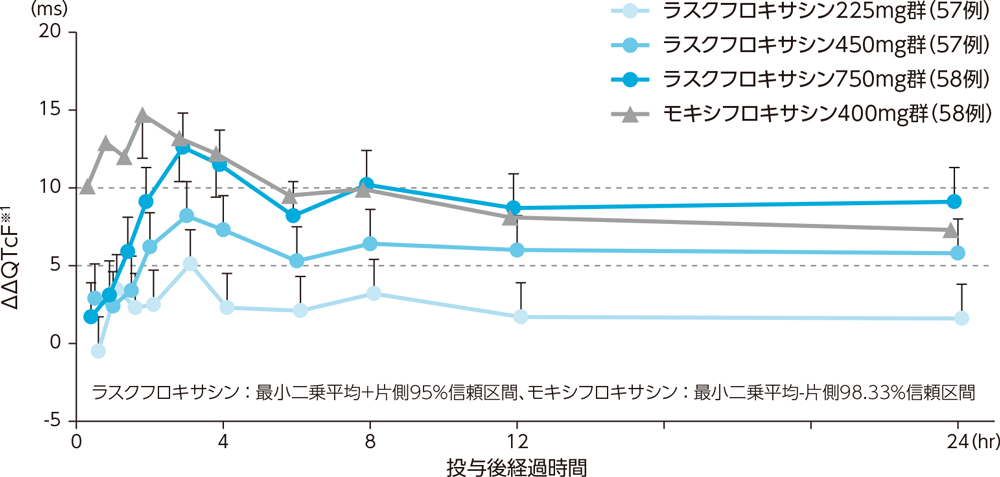
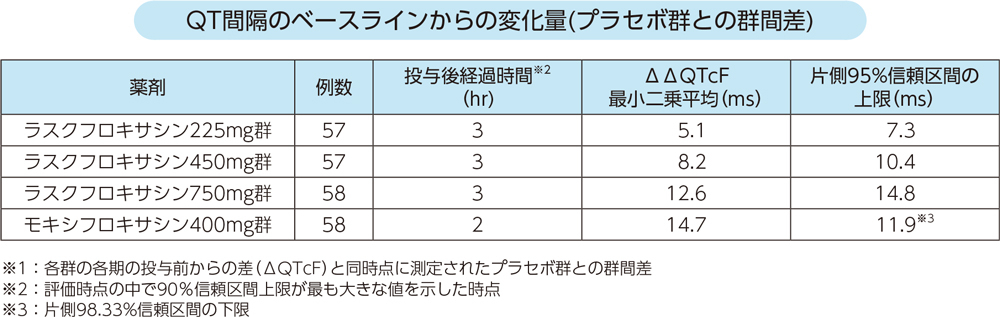
健康成人のべ172例を対象とした無作為化二重盲検クロスオーバー試験において、ラスクフロキサシン225mg(57例)、450mg(57例)及び750mg(58例)単回経口投与時のQT/QTc延長をQTcF(Fridericia法による心拍数補正QT)を用いて評価した結果、225mg投与群が陰性、450mg投与群以上で陽性と判定されたa。
a:ΔΔQTcFの最小二乗平均の片側95%信頼区間上限値がすべての時点で10ms未満であれば、QTcFの延長は陰性と判定した。
通常、成人には、ラスクフロキサシンとして1回75mgを1日1回経口投与する。
9. 特定の背景を有する患者に関する注意〈抜粋〉
9.1 合併症・既往歴等のある患者
- 9.1.2
- 重篤な心疾患(不整脈、虚血性心疾患等)のある患者
QT延長を起こすおそれがある。[11.1.4参照]
非臨床試験2)
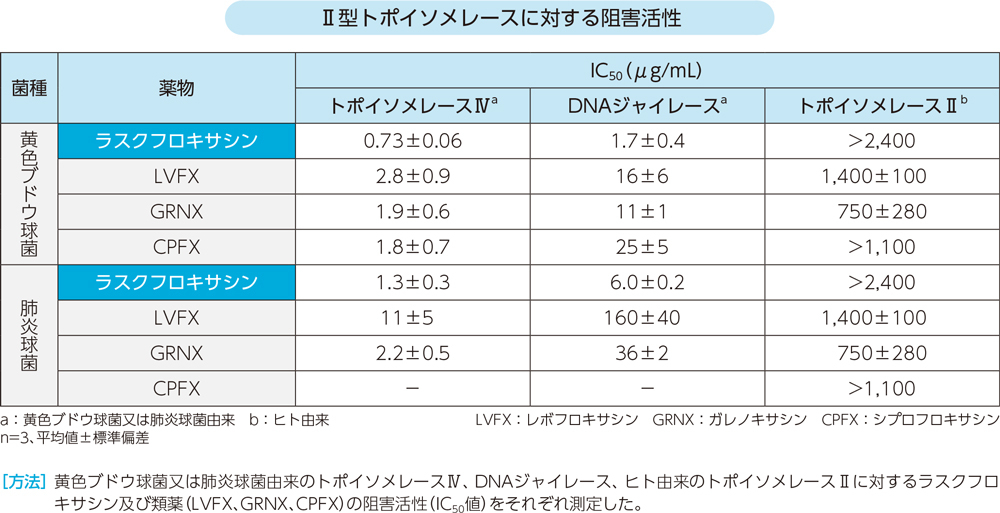
(1)細菌とヒトのⅡ型トポイソメレースに対する選択性(in vitro)
ラスクフロキサシンのヒトトポイソメレースⅡに対する阻害活性(IC50)は>2,400μg/mL、細菌のⅡ型トポイソメレース(トポイソメレースⅣ及びDNAジャイレース)に対する阻害活性は6.0±0.2μg/mL以下であった。
(2)抗菌力(in vitro)
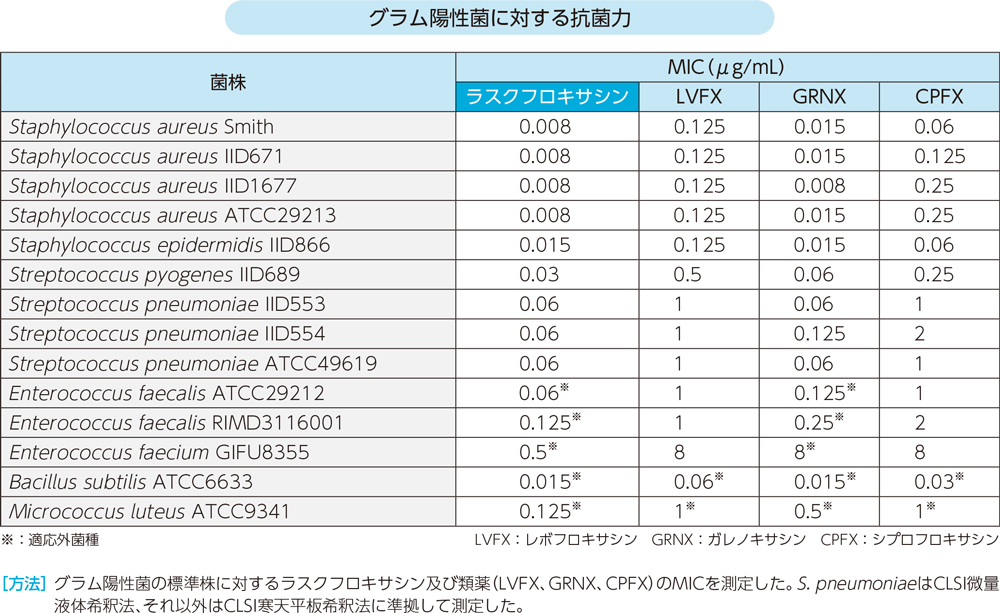
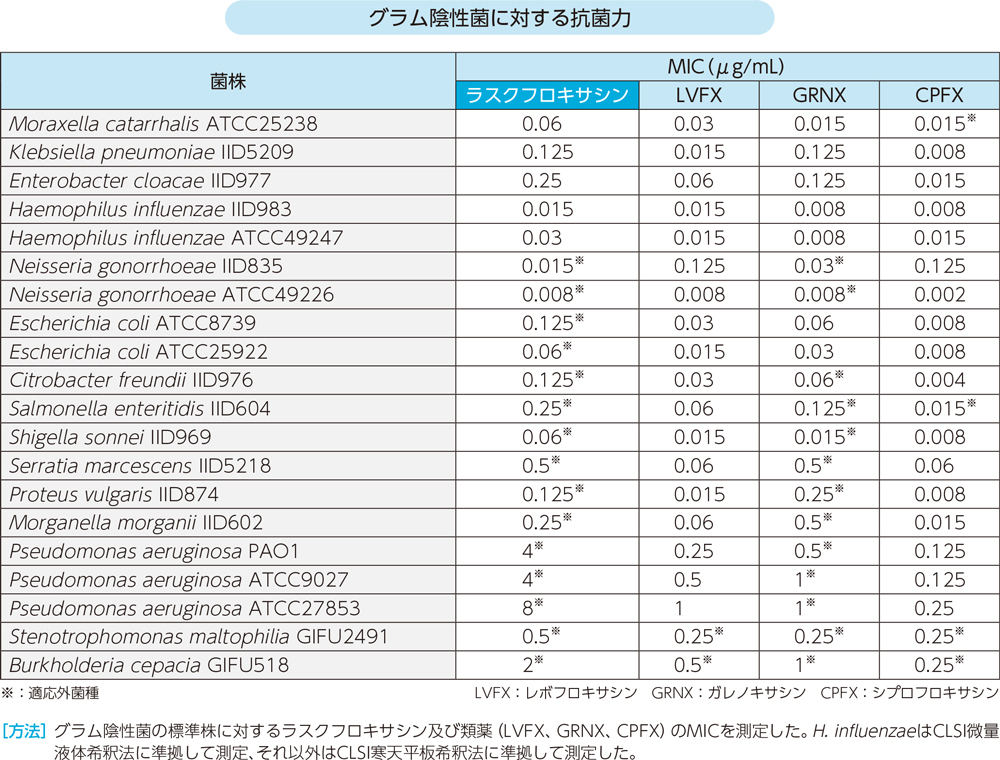
1)標準株に対する抗菌スペクトル
ラスクフロキサシンはグラム陽性菌及び陰性菌、嫌気性菌、非定型菌に対して以下の抗菌力を示した。
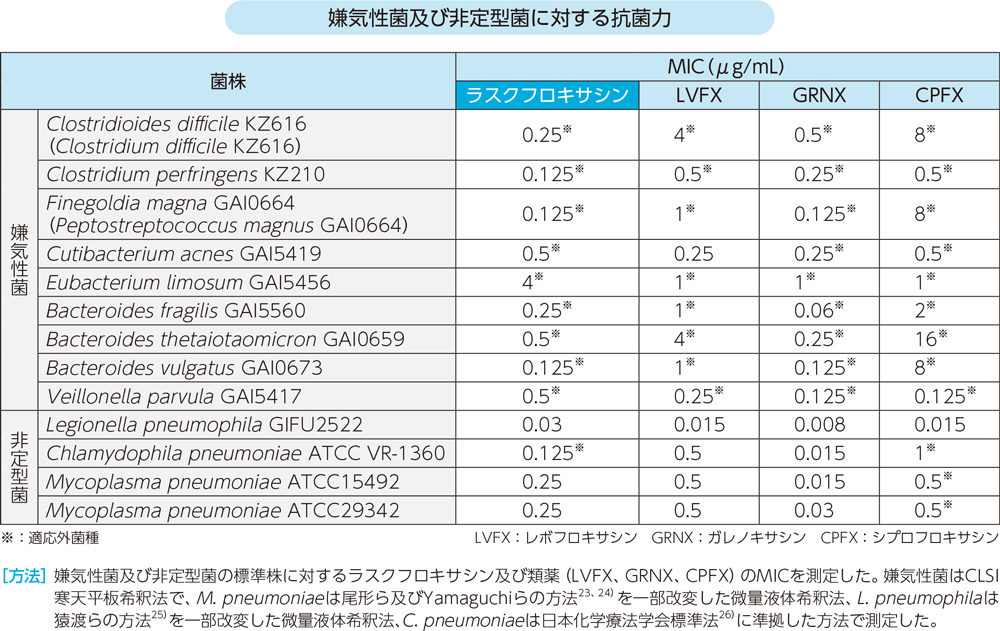
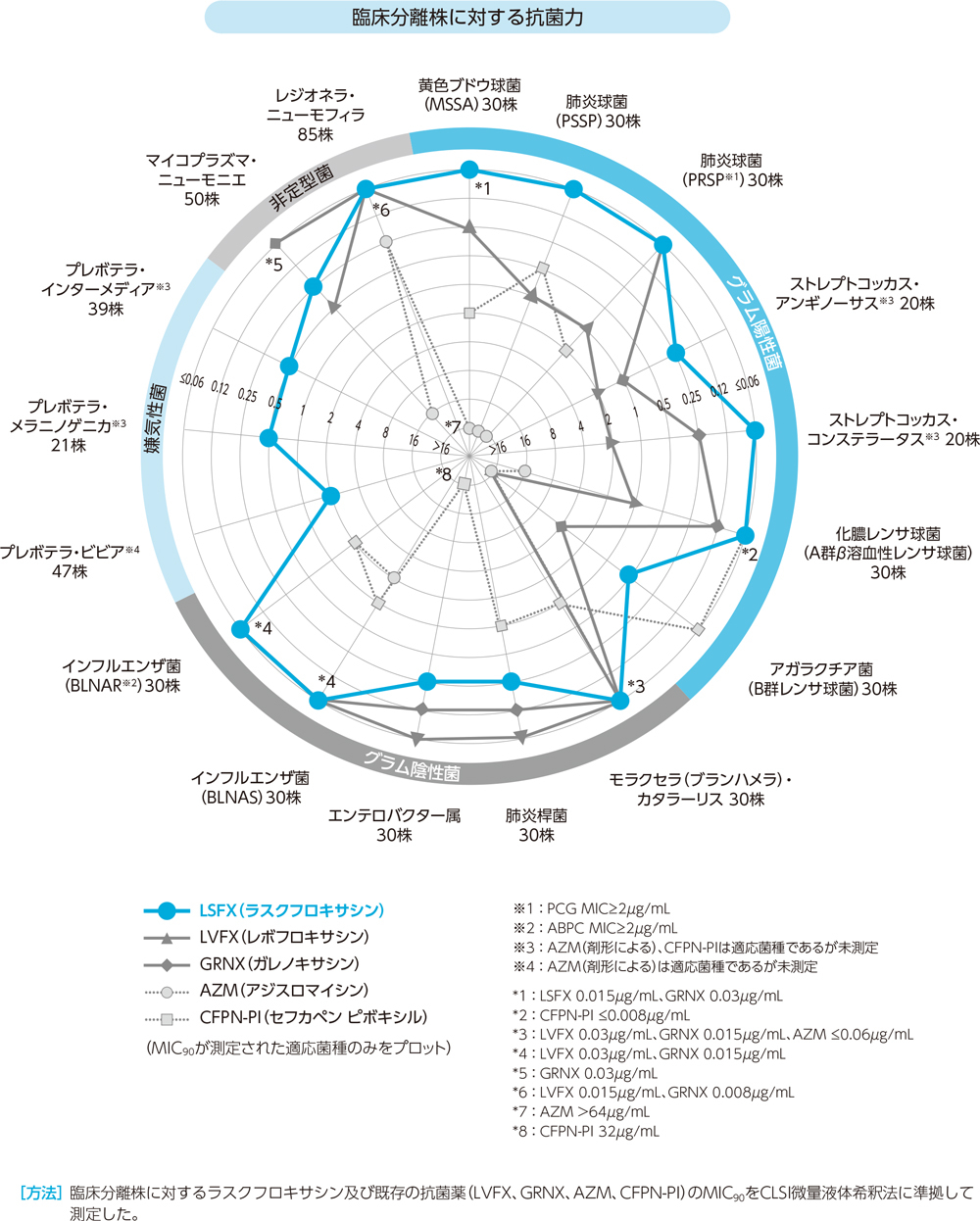
2)臨床分離株に対する抗菌力[MIC90](in vitro)
ラスクフロキサシンはグラム陽性菌及び陰性菌、嫌気性菌、非定型菌に対し、以下の抗菌力を示した。
3)キノロン標的酵素変異株に対する抗菌力(in vitro)
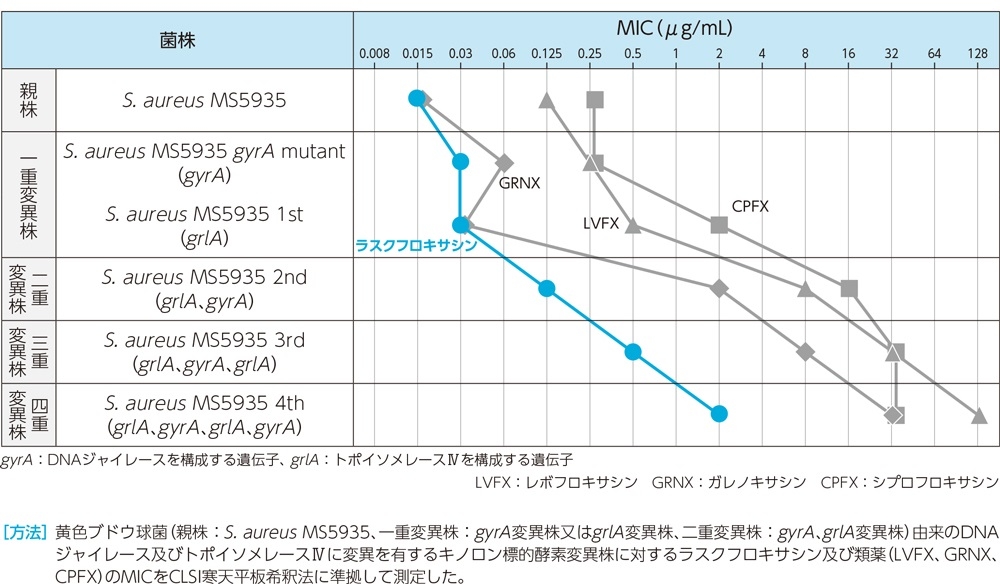
①黄色ブドウ球菌
段階的に標的酵素遺伝子に変異を加えた黄色ブドウ球菌に対するラスクフロキサシンの抗菌力は以下のとおりであり、四重変異株に対するMICは2μg/mLであった。
②肺炎球菌
段階的に標的酵素遺伝子に変異を加えた肺炎球菌に対するラスクフロキサシンの抗菌力は以下のとおりであり、二重変異株に対するMICは0.25、0.5μg/mLであった。

(3)耐性菌出現頻度(in vitro)
ラスクフロキサシンの耐性菌出現頻度は、黄色ブドウ球菌で2.1×10-9未満、肺炎球菌で1.1×10-8未満であり、試験した濃度範囲において耐性菌は選択されなかった。
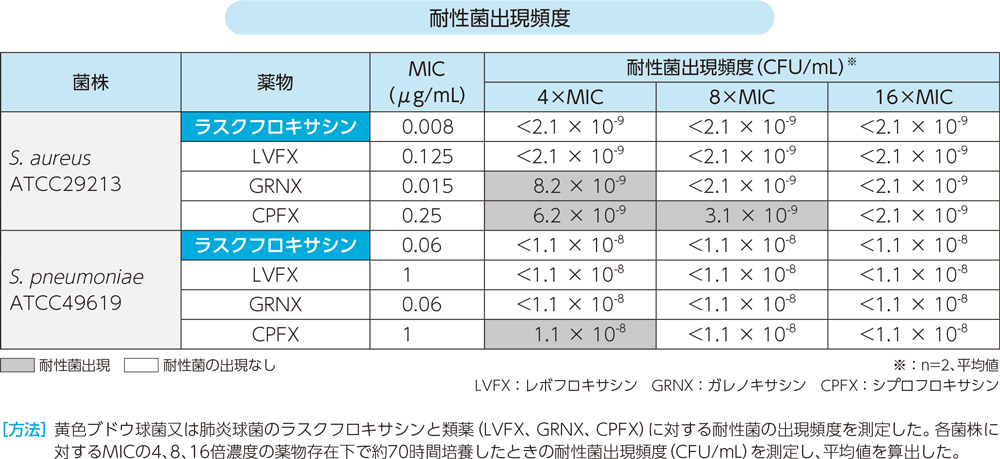
(4)耐性獲得試験(in vitro)
黄色ブドウ球菌及び肺炎球菌を7回継代培養したとき、ラスクフロキサシンのMIC上昇は継代前と比べ4倍であった。
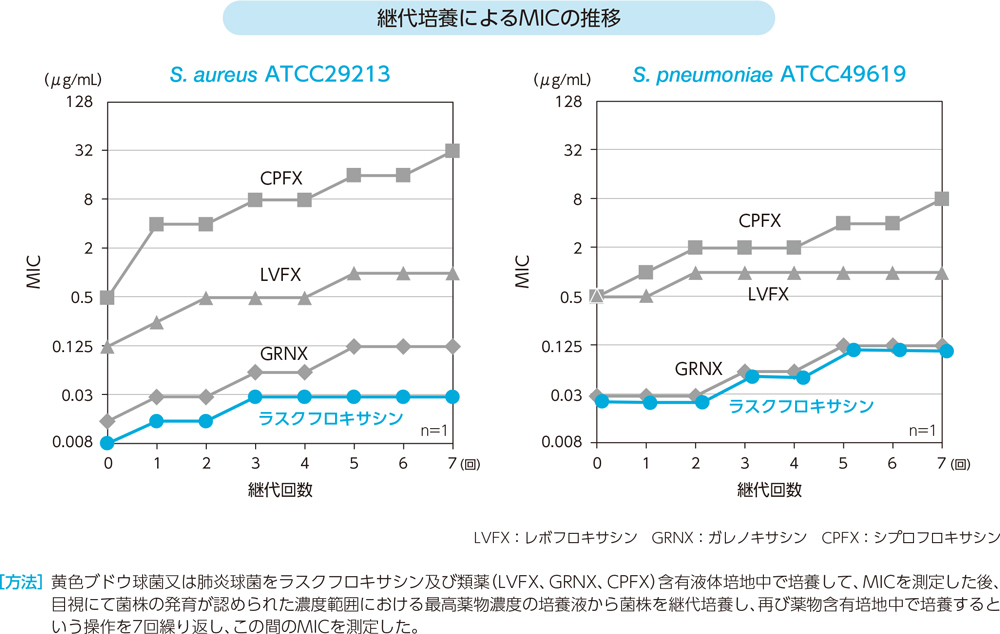
(5)肺炎球菌によるマウス肺感染モデルに対する治療効果(マウス)
ラスクフロキサシンは、コントロールと比較し、用量依存的に肺内の肺炎球菌数を有意に減少させた。
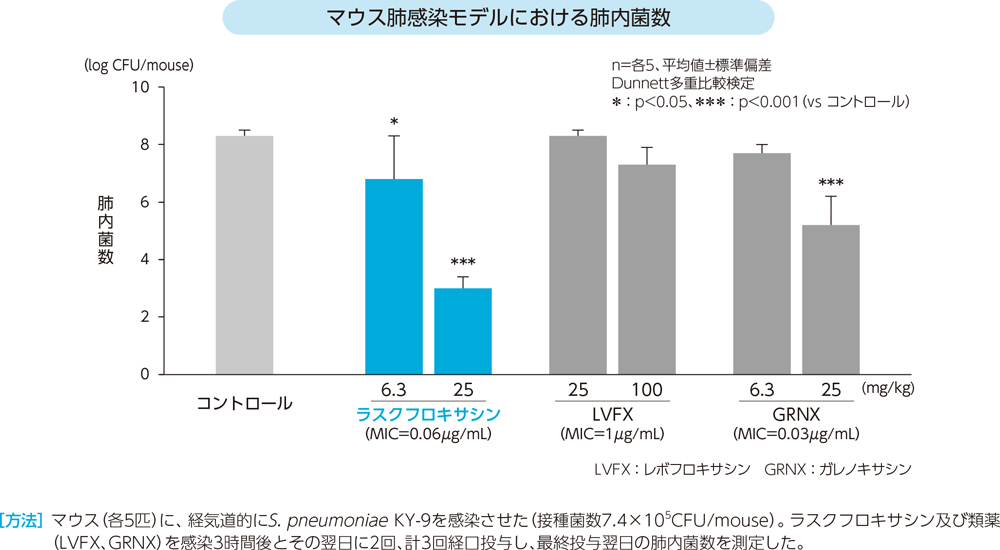
(6)肺炎球菌によるマウス肺感染モデルの肺内菌数の経時的推移(マウス)
ラスクフロキサシンは、投与後5時間でほぼ検出限界に達し、コントロールと比較し投与2時間後から24時間後まで肺内の肺炎球菌数を有意に減少させた。
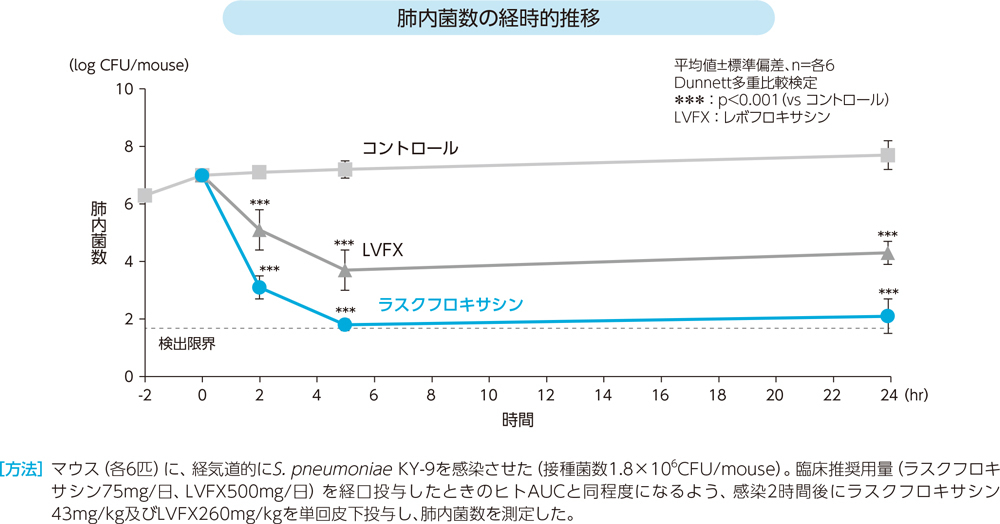
(7)PK/PD(AUC0-24/MIC90)3)
ラスビック®錠75mgを呼吸器感染症患者に反復経口投与したときのAUC0-24と臨床分離株に対するMIC90の比(AUC0-24/MIC90)は、以下のとおりであった。
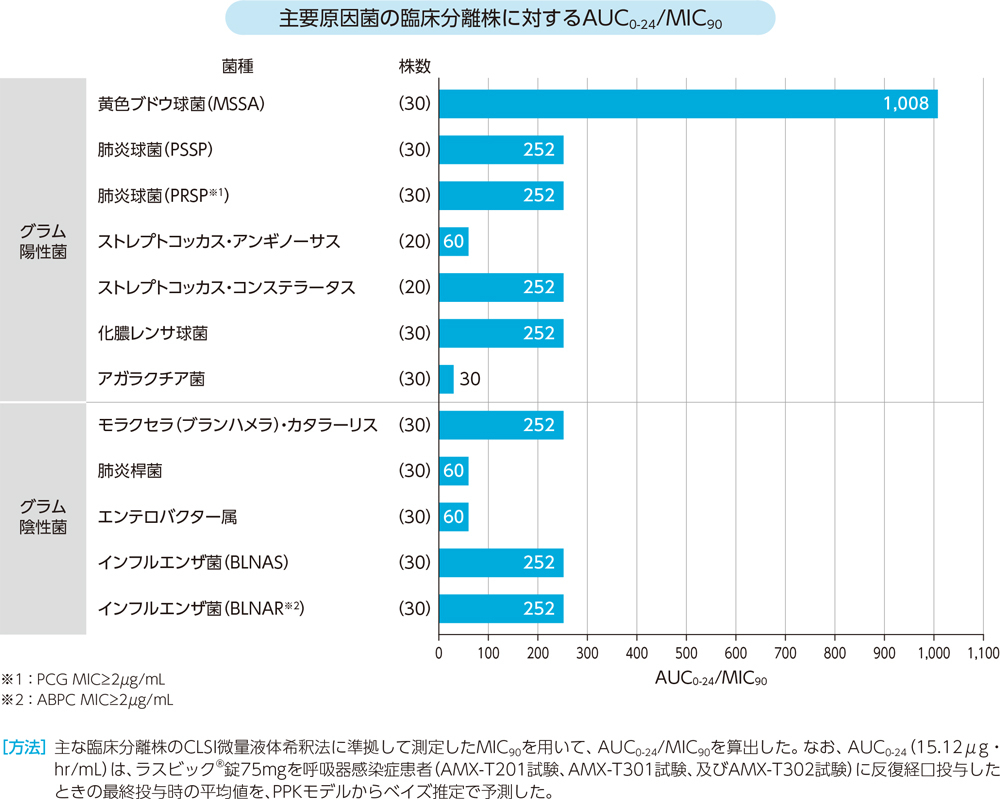
(8)耐性化リスクの検討
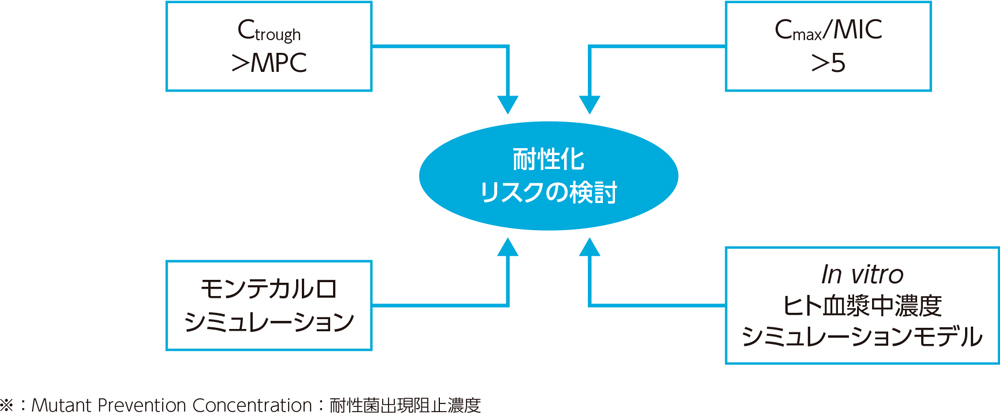
肺炎球菌においては、Cmax/MICが5未満の場合のみキノロン耐性菌が選択されたとの報告がある4)。また、MPCとMICの間の範囲はMSW(Mutant Selection Window:耐性菌選択域)と呼ばれ、MSWの範囲内では耐性菌を発現させる可能性が高くなることが報告されている5)。
これらをもとに、ラスビック®5mg1日1回経口投与における肺炎球菌の耐性化リスクについて検討した。
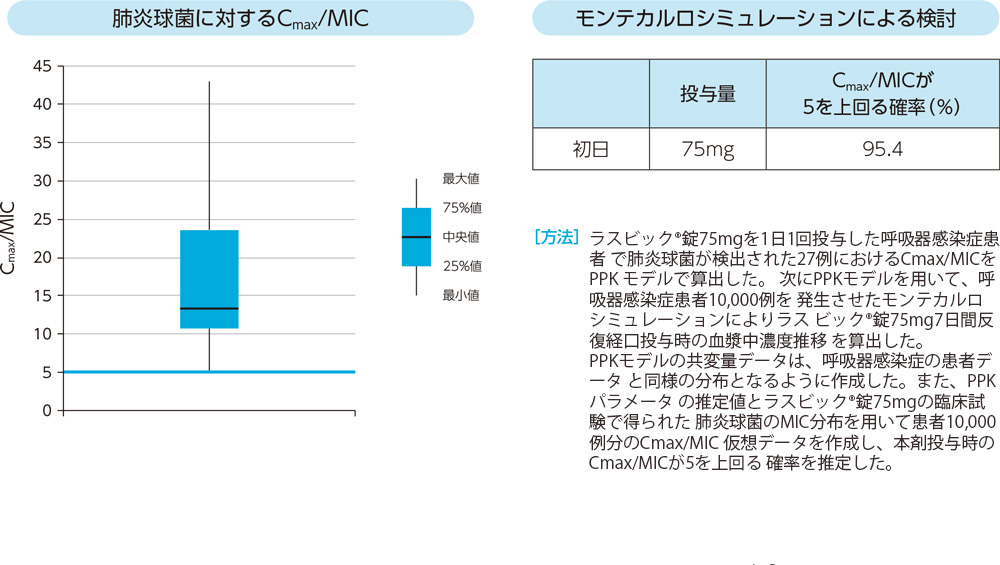
1)Cmax/MIC6)、7)、8)
ラスビック®錠75mgを1日1回経口投与した呼吸器感染症患者で肺炎球菌が検出された27例全例において、Cmax/MICが5を上回った。またモンテカルロシミュレーションを用いた検討から、投与初日にCmax/MICが5を上回る確率は95.4%であった。
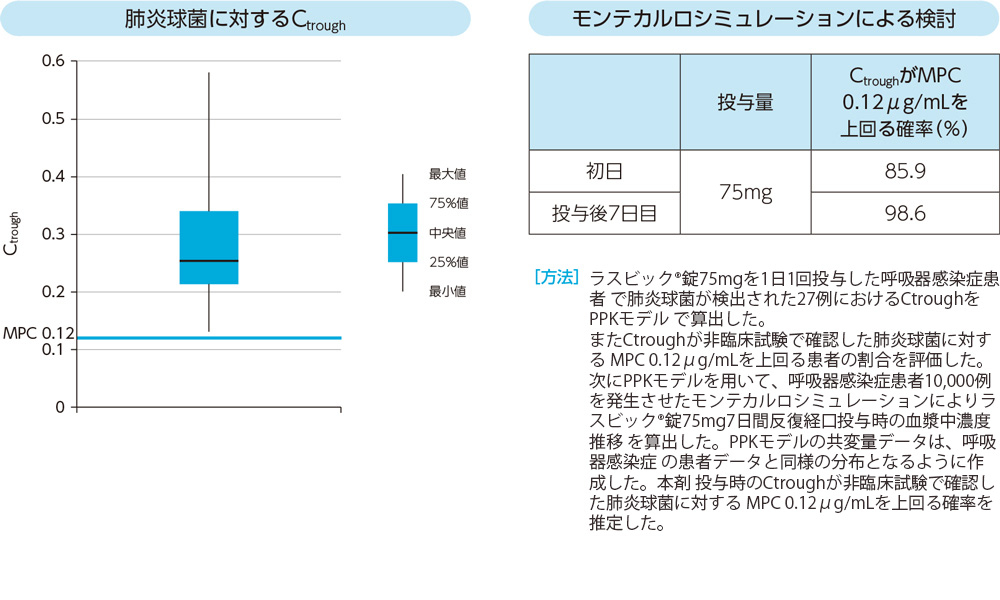
2)Ctrough6)、7)、8)
ラスビック®錠75mgを1日1回経口投与した呼吸器感染症患者で肺炎球菌が検出された27例全例において、Ctroughが0.12μg/mLを上回った。またモンテカルロシミュレーションを用いた検討から、Ctroughが肺炎球菌のMPC 0.12μg/mLを上回る確率は、投与初日が85.9%、投与後7日目が98.6%であった。
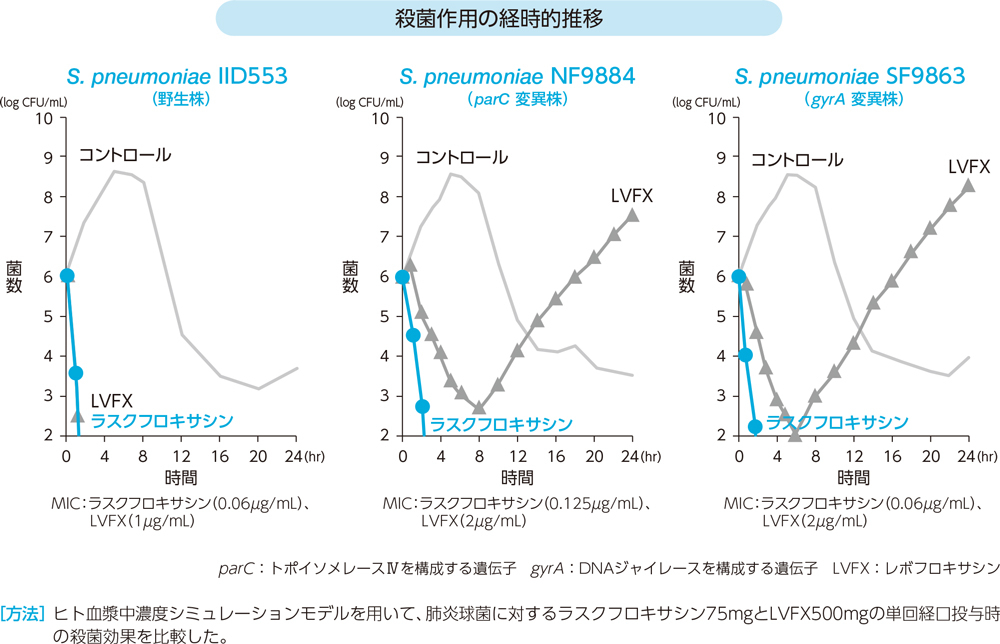
3)ヒト血漿中濃度シミュレーションモデルにおける肺炎球菌に対する殺菌作用(in vitro)2)
ラスクフロキサシンは、肺炎球菌の野生株及びキノロン標的酵素変異株に対し、シミュレーション開始3時間後までに検出限界以下に殺菌し、24時間後に再増殖した株は認められなかった。
- 1)承認時評価資料:ラスクフロキサシンの臨床薬理試験.
- 2)承認時評価資料:ラスクフロキサシンの薬効薬理試験.
- 3)社内資料:ラスクフロキサシン投与時のPK-PDパラメータ
- 4)Madaras-Kelly KJ, et al., Diagn Microbiol Infect Dis. 37(4): 253-260(2000)
- 5)戸塚恭一 三鴨廣繁 監修, 日常診療に役立つ抗感染症薬のPK-PD. ユニオンエース(2010)
- 6)承認時評価資料:市中肺炎患者を対象とした第Ⅱ相試験(用量設定試験)(AMX-T201試験).
- 7)承認時評価資料:市中肺炎患者を対象とした第Ⅲ相二重盲検比較試験(AMX-T301試験).
- 8)承認時評価資料:呼吸器感染症患者を対象とした第Ⅲ相非盲検非対照試験(AMX-T302試験).
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

