-薬物動態-
血中濃度1)
(1)単回投与
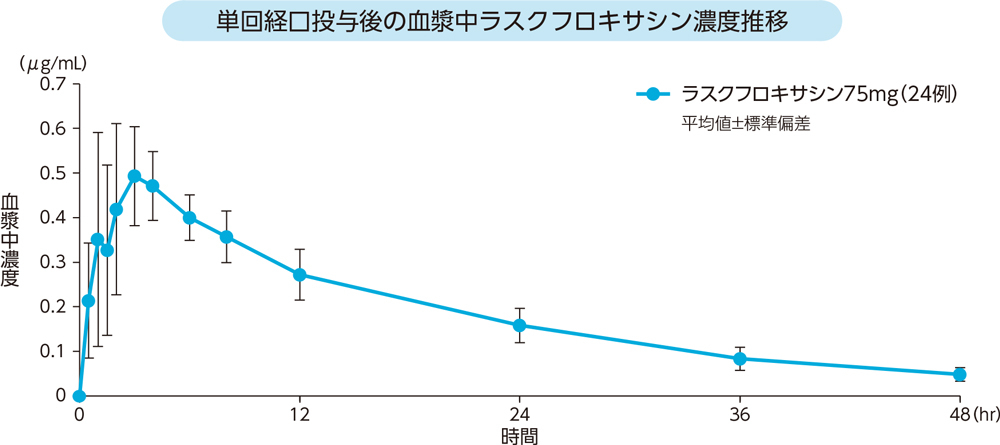
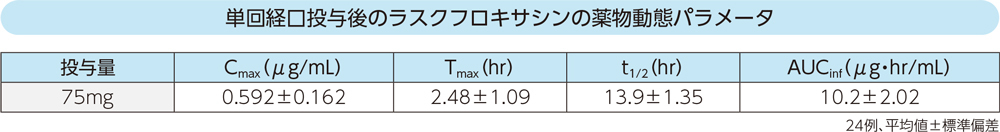
健康成人24例にラスクフロキサシン75mgを空腹時単回経口投与したときの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。
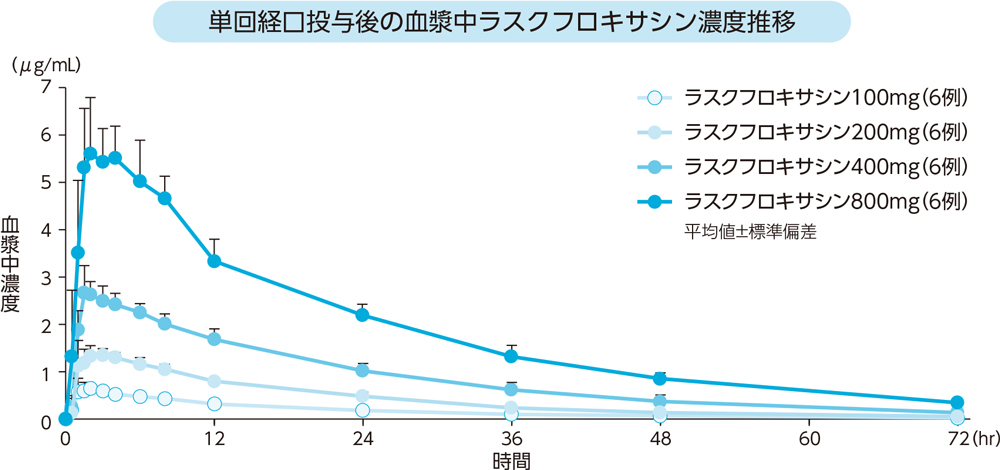
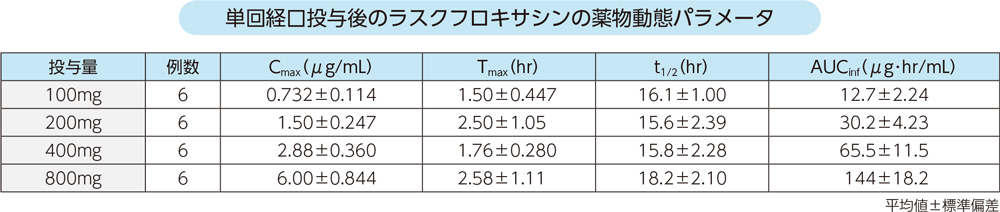
健康成人各6例にラスクフロキサシン100mg、200mg、400mg、800mgを空腹時単回経口投与したときの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。
通常、成人には、ラスクフロキサシンとして1回75mgを1日1回経口投与する。
(2)反復投与
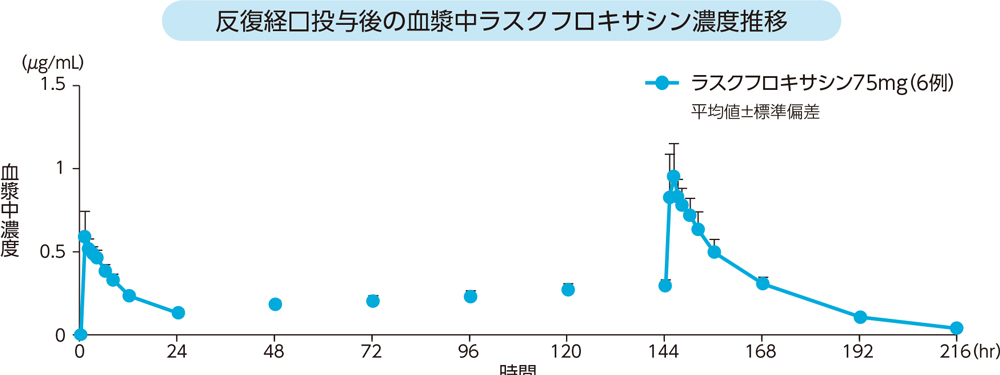
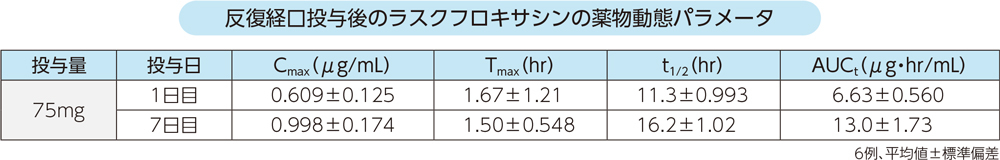
健康成人6例にラスクフロキサシン75mgを1日1回7日間空腹時反復経口投与したときの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。ラスクフロキサシンの血漿中濃度は投与開始7日目までにほぼ一定となった。
(3)食前/食後投与
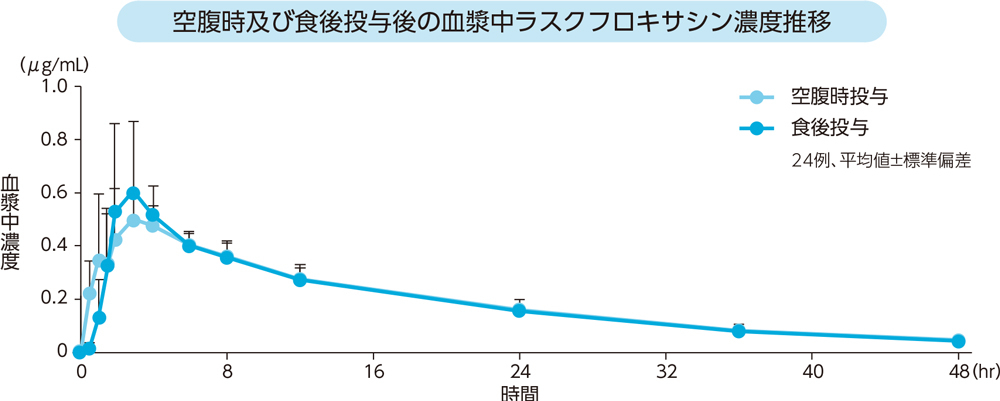
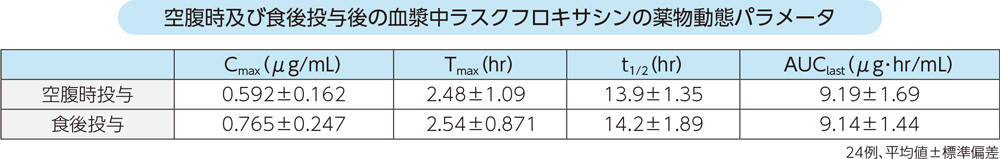
健康成人24例に空腹時及び食後にラスクフロキサシン75mgを単回経口投与したときの血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。
(4)感染症患者
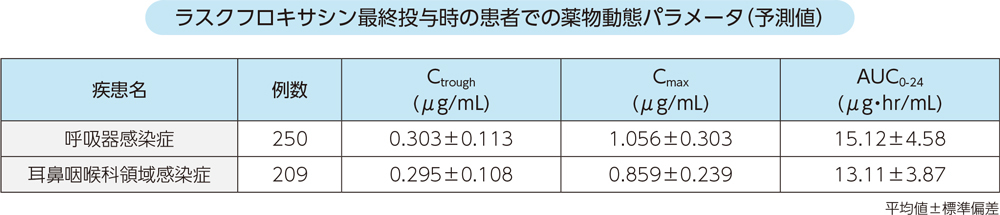
母集団薬物動態モデルから予測した、感染症患者にラスクフロキサシン75mg1日1回反復投与したときの投与終了時の薬物動態パラメータは以下のとおりであった。
(5)腎機能障害者
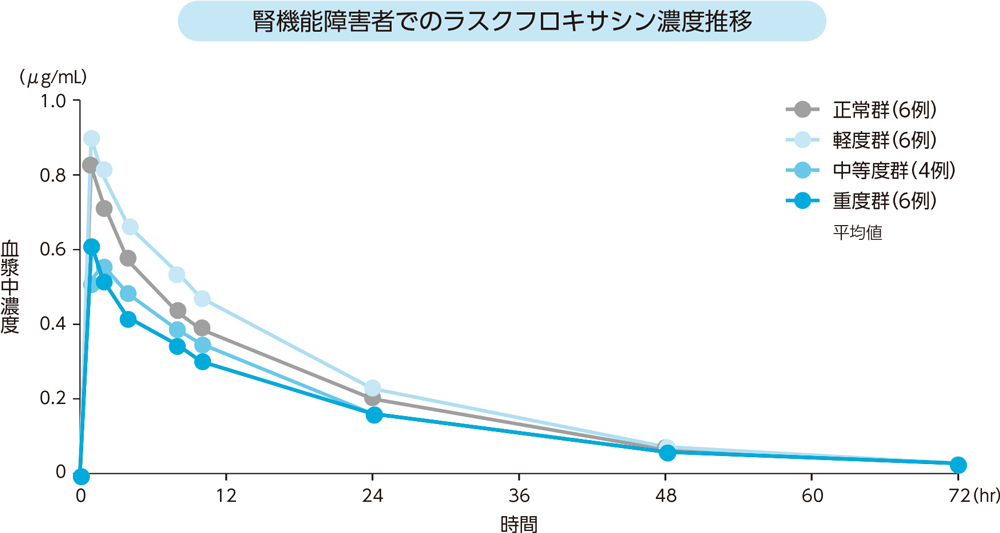
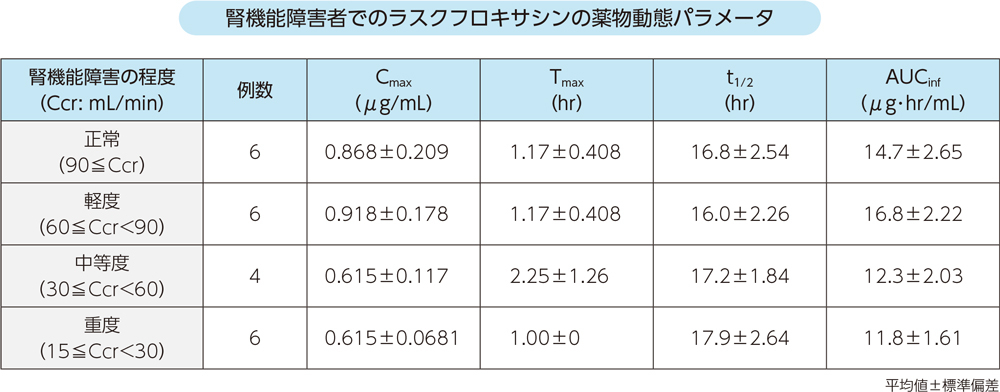
腎機能障害者にラスクフロキサシン75mgを単回経口投与したとき、血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。
(6)肝機能障害者
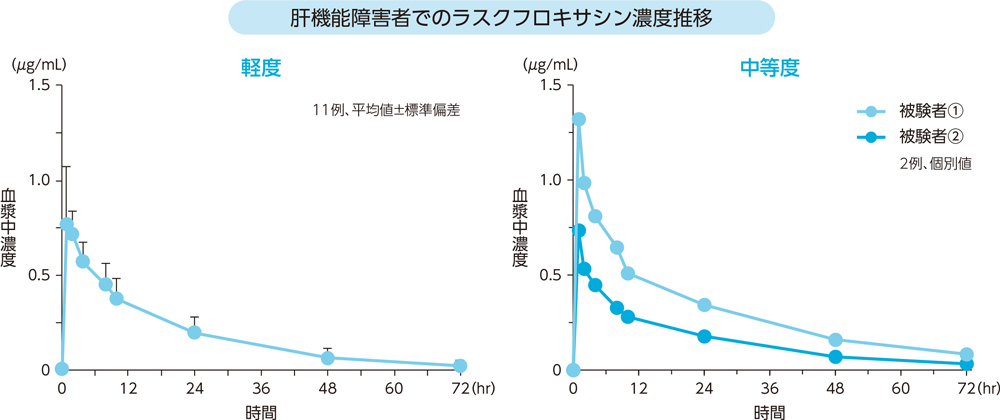
肝機能障害が軽度及び中等度の患者にラスクフロキサシン75mgを単回経口投与したとき、血漿中濃度推移及び薬物動態パラメータは以下のとおりであった。
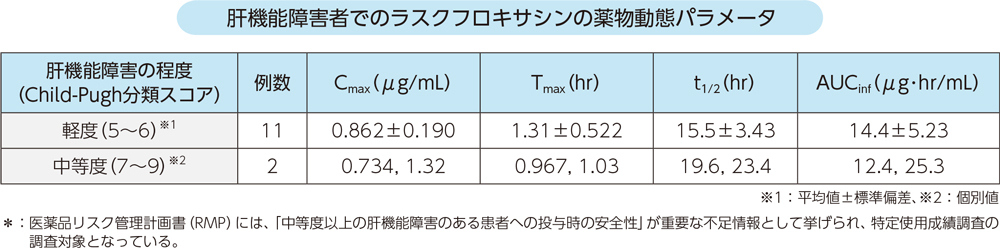
9.3 肝機能障害患者
- 9.3.1
- 中等度以上の肝機能障害のある患者
血漿中濃度上昇のおそれがある。[16.6.2参照]
(7)高齢者
高齢者(6例:66~79歳)及び非高齢者(6例:32~36歳)にラスクフロキサシン200mgを単回経口投与したときの血漿中ラスクフロキサシンの薬物動態パラメータは以下のとおりであった。
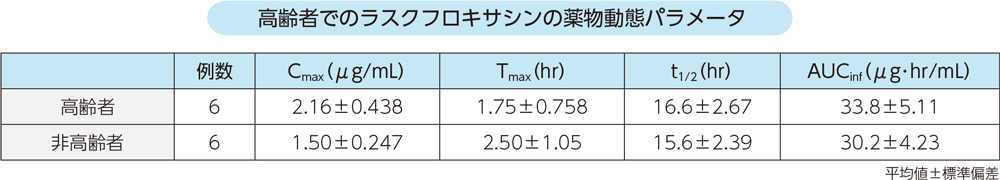
通常、成人には、ラスクフロキサシンとして1回75mgを1日1回経口投与する。
9. 特定の背景を有する患者に関する注意〈抜粋〉
9.8 高齢者
- 9.8.1
- 腱障害があらわれやすいとの報告がある。
- 9.8.2
- 患者の状態を十分に観察しながら慎重に投与すること。一般に高齢者では生理機能が低下している。本剤の臨床試験成績では、高齢者(65~88歳)において認められた副作用の種類及びその発現率は、非高齢者(16~64歳)と同様であった。
分布
(1)組織移行性1)
1)肺組織
健康成人30例(各時間6例)にラスクフロキサシン75mgを単回経口投与後1~24時間での対血漿中濃度比は、肺胞上皮被覆液で平均15.0~22.4、肺胞マクロファージで平均18.5~56.4であった。
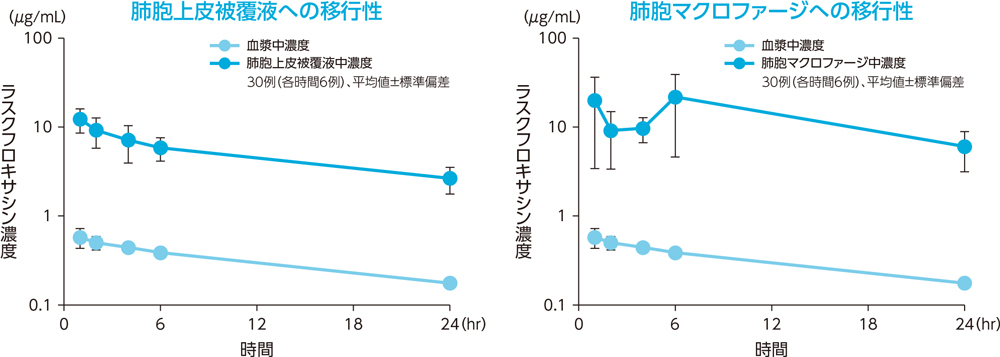
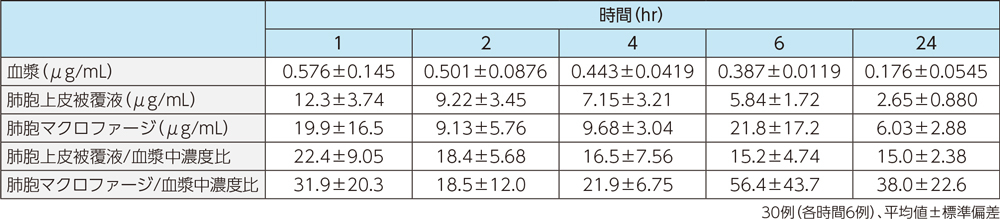
2)喀痰
呼吸器感染症患者36例にラスクフロキサシン75mgを経口投与後1~3時間での対血漿中濃度比は喀痰で0.613±0.289(平均値±標準偏差)であった。
3)耳鼻咽喉組織
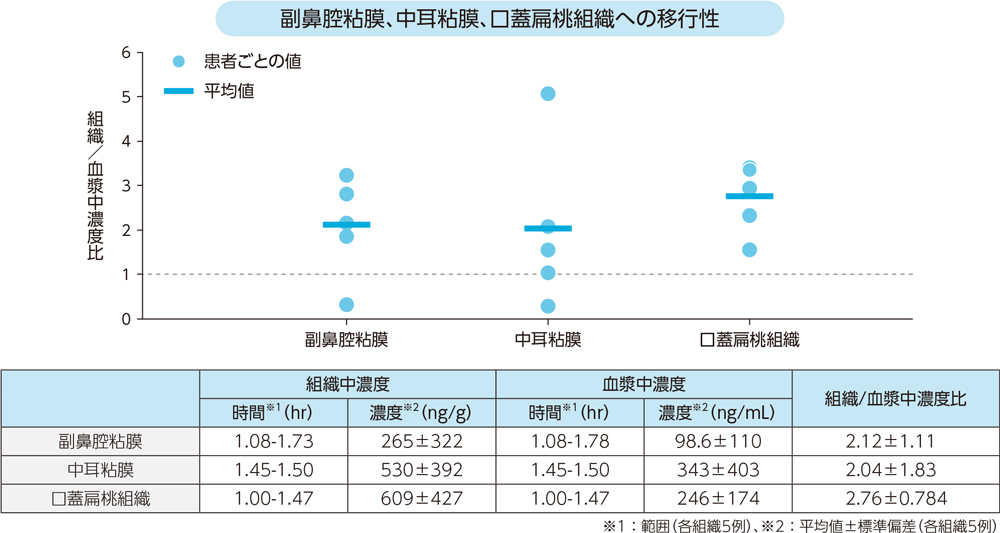
耳鼻咽喉組織摘出術施行患者(各組織5例)にラスクフロキサシン75mgを単回経口投与後1~2時間での対血漿中濃度比(平均値±標準偏差)は、副鼻腔粘膜2.12±1.11、中耳粘膜2.04±1.83、口蓋扁桃組織2.76±0.784であった。
(2)蛋白結合率(in vitro2))
ラスクフロキサシン1~10μg/mLの in vitro でのヒト血漿蛋白結合率は71.2~74.0%であった。
代謝(in vitro2)、健康成人1))
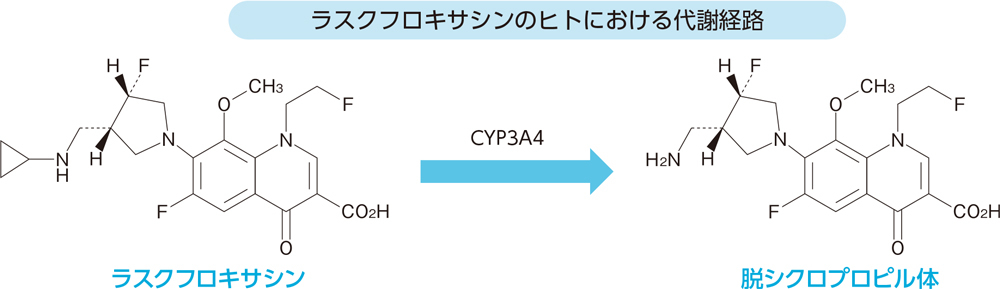
In vitroにおいてラスクフロキサシンはCYP3A4により脱シクロプロピル体に代謝された。
健康成人にラスクフロキサシン75mgを単回経口投与したとき、血漿中には主に未変化体が検出され、その他に脱シクロプロピル体が検出された。
排泄1)
健康成人にラスクフロキサシン75mgを単回経口投与したとき、投与後144時間までの未変化体の排泄率は、尿中に8.38%、糞中に16.0%であった。未変化体と脱シクロプロピル体の排泄率の合計は、尿中に39.9%、糞中に24.9%であった。
薬物相互作用(in vitro2)、健康成人1))
(1)In vitro試験成績
ヒト肝ミクロソームを用いてCYP分子種の代謝活性に対するラスクフロキサシンの阻害効果を検討したところ、ラスクフロキサシンはCYP3A4及びCYP2C8を時間依存的に阻害した。ヒト凍結肝細胞を用いてCYP分子種に対するラスクフロキサシンの誘導能を検討したところ、CYP1A2及びCYP3A4に対する誘導作用が認められた。また、各種トランスポータ発現細胞を用いてラスクフロキサシンの基質性を検討したところ、ラスクフロキサシンはP-糖タンパクの基質であった。同様にラスクフロキサシンの各種トランスポータに対する阻害効果を検討したところ、ラスクフロキサシンはMATE1及びMATE2-K発現細胞の基質輸送を阻害した。
(2)臨床試験成績
1)制酸剤との併用
健康成人9例に乾燥水酸化アルミニウムゲル(1,075.2mg)・水酸化マグネシウム(960mg)の配合剤とラスクフロキサシン75mgを併用投与したとき、ラスクフロキサシンのCmax及びAUClastはそれぞれ0.513倍及び0.681倍に減少した。
2)ファモチジンとの併用
健康成人9例に、ファモチジン20mgとラスクフロキサシン75mgを併用投与したとき、ラスクフロキサシンのCmax及びAUClastに変化はなかった。
3)イトラコナゾールとの併用
健康成人5例にイトラコナゾール200mgとラスクフロキサシン75mgを併用投与したとき、ラスクフロキサシンのCmax及びAUClastはそれぞれ1.16倍及び1.46倍に増加した。
4)フェロジピンとの併用
健康成人12例にフェロジピン2.5mgとラスクフロキサシン200mgを併用投与したとき、フェロジピンのCmax及びAUClastはそれぞれ1.15倍及び1.62倍に増加した。
5)テオフィリンとの併用
健康成人6例にテオフィリン200mgとラスクフロキサシン150mgを併用投与したとき、テオフィリンのCmax及びAUC0-10はそれぞれ1.17倍及び1.18倍に増加した。
6)モンテルカストとの併用
健康成人10例にモンテルカスト5mgとラスクフロキサシン150mgを併用投与したとき、モンテルカストのCmax及びAUClastはそれぞれ1.41倍及び1.94倍に増加した。
7)メトホルミンとの併用
健康成人8例に、メトホルミン250mgとラスクフロキサシン150mgを併用投与したとき、メトホルミンのCmax及びAUClastに変化はなかった。
通常、成人には、ラスクフロキサシンとして1回75mgを1日1回経口投与する。
- 1)承認時評価資料:ラスクフロキサシンの臨床薬理試験.
- 2)承認時評価資料:ラスクフロキサシンの薬物動態試験.
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

