-安全性-
安全性薬理試験1)
1. 一般症状及び行動に及ぼす影響(マウス)
メサラジンは100mg/kg、300mg/kgの経口投与において、マウスの一般症状及び行動に影響を及ぼしませんでした。1000mg/kgでは一部の例(6例中1〜4例)で一過性の興奮に伴う反応性の増大と触覚反応、痛覚反応及び耳介反射の亢進が認められましたが、投与後180分には消失し回復が認められました。
2. 中枢神経系に及ぼす影響(マウス、ラット)
マウスの自発運動に対してメサラジン100mg/kg、300mg/kgの経口投与では影響がありませんでしたが、1000mg/kgでは投与後15〜30分に軽度な自発運動量の減少傾向が見られました。メサラジンは1000mg/kgまでの経口投与において、マウスを用いた麻酔作用、抗けいれん作用、けいれん誘発作用、鎮痛作用には影響を及ぼさず、ラットの体温にも影響を及ぼしませんでした。
3. 自律神経系及び平滑筋に及ぼす影響(in vitro)
メサラジンは1×10−6、1×10−5及び1×10−4Mの濃度でウサギの摘出回腸の自動運動に影響を及ぼさず、モルモット摘出回腸でのアセチルコリン、ヒスタミン、塩化バリウムによる収縮にも影響を及ぼしませんでした。
4. 呼吸・循環器系に及ぼす影響(イヌ)
メサラジンは100mg/kg、300mg/kg及び1000mg/kgの十二指腸内投与により、麻酔イヌの呼吸数、血圧、心拍数、大腿動脈血流量、心電図に影響を及ぼしませんでした。
5. 消化器系に及ぼす影響(マウス、ラット)
メサラジンは100mg/kg、300mg/kg及び1000mg/kgの経口投与においてマウスでの小腸輸送能に影響を及ぼさず、ラットでの胃内容物排泄能及び胃液分泌にも影響を及ぼしませんでした。
6. 水及び電解質代謝に及ぼす影響(ラット)
メサラジンは100mg/kgの経口投与ではラットの尿量及び尿中電解質排泄量に影響を及ぼしませんでした。300mg/kgの経口投与では尿中ナトリウム及び塩素イオン排泄量の増加並びに尿量及び尿中カリウムイオン排泄量の増加傾向が認められました。1000mg/kgの経口投与では尿量並びに尿中ナトリウム、カリウム及び塩素イオン排泄量の増加が認められました。
7. その他に及ぼす影響(ラット、in vitro)
メサラジンは100mg/kg、300mg/kg及び1000mg/kgの経口投与ではラットの血液凝固系に影響を及ぼしませんでした。また、メサラジンは1×10−6、1×10−5及び1×10−4Mの濃度でウサギの血小板凝集に影響を及ぼさず、ウサギ赤血球に対しても1×10−6、1×10−5及び1×10−4Mの濃度で溶血作用を示しませんでした。
毒性試験2)
1. 単回投与毒性(ラット、サル)

2. 反復投与毒性(ラット、サル)
CD系ラットを用いた13週間(休薬13週間)5)及び52週間投与試験、カニクイザルを用いた13週間及び1年間投与試験をそれぞれ経口投与により行いました。いずれの試験においても高用量では腎毒性が認められました。無毒性量はラットでは100〜800mg/kg、カニクイザルでは125〜250mg/kgで、これらは臨床用量のそれぞれ2〜32倍、2.5〜10倍でした。
3. 生殖・発生毒性(ラット、ウサギ)6)
経口投与により、ラットを用いた妊娠前、妊娠期及び授乳期投与試験、ラット及びウサギを用いた器官形成期投与試験、ラットを用いた周産期及び授乳期投与試験を行い、更にラットを用いた器官形成期、周産期及び授乳期投与試験を実施しました。その結果、雌雄の生殖能力、胎児の発育・次世代への影響はなく、催奇形性も認められませんでした。
4. 抗原性(モルモット、マウス)7)
モルモット及びマウスを用いた全身性アナフィラキシー反応(ASA反応)あるいは皮膚アナフィラキシー反応(PCA反応)試験を行いました。いずれの試験においてもメサラジンに抗原性は認められませんでした。
5. 変異原性(in vitro、マウス)8)
大腸菌及びサルモネラ菌を用いた復帰突然変異試験、チャイニーズハムスター肺由来線維芽細胞(CHL/IU)を用いた染色体異常試験、マウスの小核試験を行いました。その結果、変異原性は認められませんでした。
6. がん原性(マウス、ラット)
マウス及びラットを用いた混餌投与による104週間がん原性試験を行いました。いずれの動物においてもがん原性を示唆する所見は認められませんでした。
7. 代謝物の単回投与毒性(ラット)
CD系ラットを用いて代謝物のN−アセチルメサラジンの静脈内投与による試験を行いました。その結果、致死量は500mg/kg以上でした。
8. 局所刺激性試験(ウサギ)
メサラジンを白色ワセリンに混入し、軟膏としてウサギに50、100mg/kgを直腸内に4週間投与したところ、ごく軽度な刺激性が認められました。同様に100mg/kgを4週間投与し、更に4週間休薬したところ、投与終了時にごく軽度な刺激性が認められましたが、休薬により回復しました。
ウサギにメサラジン注腸剤80、320mg/kgを直腸内に4週間投与したところ局所刺激性は認められませんでした。
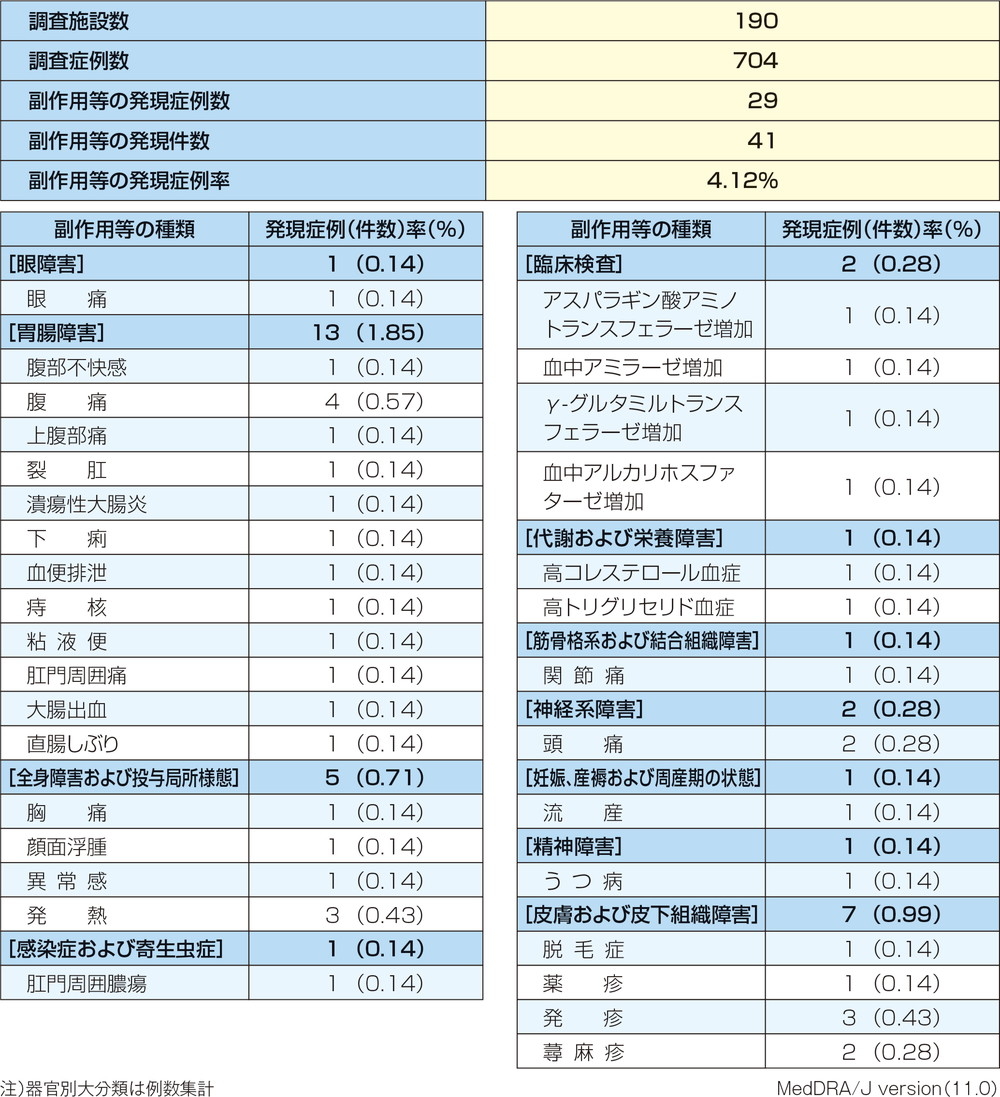
ペンタサⓇ注腸特定使用成績調査における副作用の発現状況一覧表
- 1) Kotanagi H. et al:J Gastroenterol 1998;33:571-574
- 2) ペンタサⓇ注腸1gの毒性(社内資料)
- 3) 太田隆雄 他:応用薬理 1994;47(6):505-507
- 4) 中浦槇介 他:応用薬理 1994;47(6):509-511
- 5) 木村 均 他:応用薬理 1994;48(4):277-288
- 6) 太田隆雄 他:応用薬理 1994;47(6):513-522
- 7) 和田 浩 他:応用薬理 1994;47(6):523-528
- 8) 永澤佳子 他:応用薬理 1994;48(6):501-509
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

