-薬物動態-
吸収 <外国人データ>
1. 単回投与(潰瘍性大腸炎患者)1)
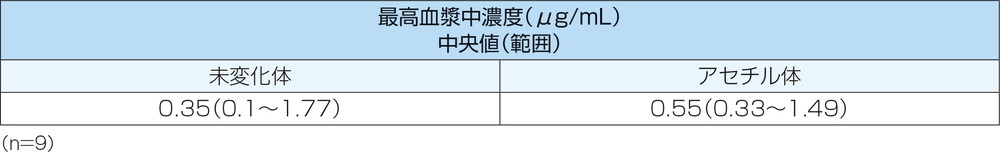
潰瘍性大腸炎患者9例にメサラジン注腸剤100mL(メサラジンとして1g含有)を単回経直腸投与したとき、血漿中未変化体及び代謝物であるN-アセチルメサラジン(アセチル体)は投与後3時間にそれぞれ0.35μg/mL(中央値、範囲0.1~1.77μg/mL)及び0.55μg/mL(中央値、範囲0.33~1.49μg/mL)の最高血漿中濃度に達しました。
【メサラジン注腸剤(1g/100mL、pH4.8)を単回投与したときの最高血漿中濃度】
2. 反復投与
①1日1回7日間反復投与(健康成人)2)
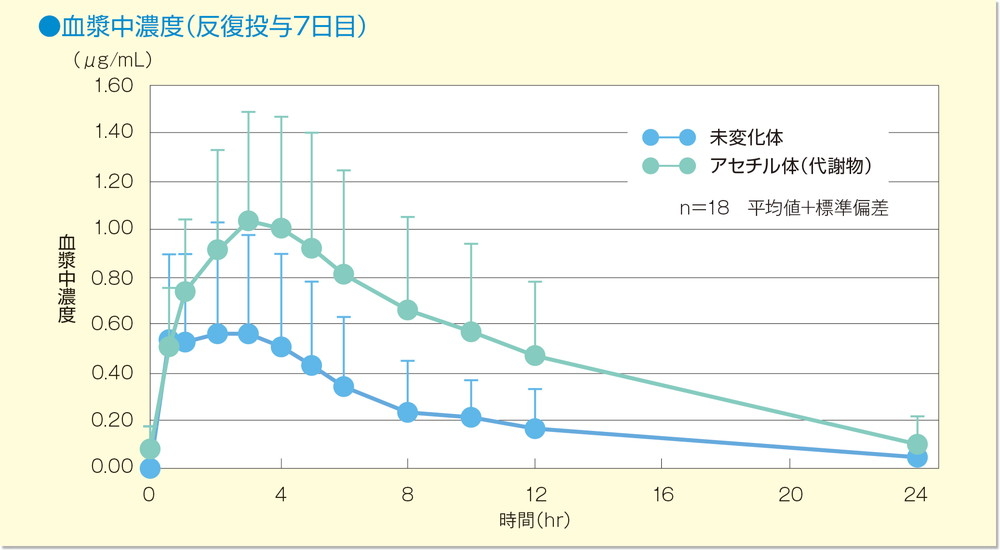
健康成人男女18名にメサラジン注腸剤(1g/100mL)を1日1回7日間反復投与し、未変化体及びアセチル体(代謝物)の血漿中濃度及び尿中排泄量を測定しました。
投与7日目の未変化体及びアセチル体(代謝物)の最高血漿中濃度(Cmax)は、それぞれ0.709及び1.122μg/mL、薬物血中濃度時間曲線下面積(AUC)はそれぞれ5.48及び12.12μg・hr/mLでした。
尿中排泄率は、投与量に対して未変化体1.31%、アセチル体(代謝物)19.12%で、尿中総排泄率は20.44%でした。
【反復投与7日目の薬物動態パラメーター】

②1日1回10日間反復投与(潰瘍性大腸炎患者)1)
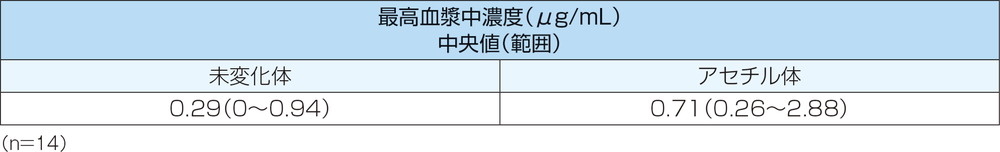
デンマークで潰瘍性大腸炎患者16例にメサラジン注腸剤(1g/100mL、pH4.8)を1日1回、10日間経直腸反復投与したとき、投与開始9日目のメサラジン未変化体とアセチル体の血漿中濃度は投与3時間後に下表に示す最高血漿中濃度に達しました。
【メサラジン注腸剤(1g/100mL、pH4.8)を反復投与したときの最高血漿中濃度】
血漿蛋白結合率(in vitro)
限外ろ過法を用いて測定したメサラジン未変化体及びアセチル体それぞれのヒトにおけるin vitro血漿蛋白結合率は以下のとおりでした。
蛋白結合率はメサラジンで約70%、アセチル体で約88%でした。
【メサラジン未変化体及びアセチル体のヒトにおけるin vitro血漿蛋白結合率(%)】
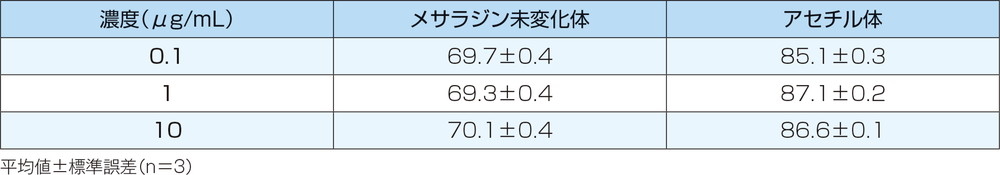
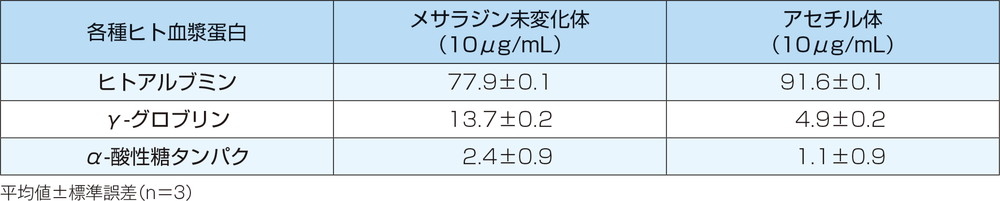
【メサラジン未変化体及びアセチル体の各種ヒト血漿蛋白への結合率(%)】
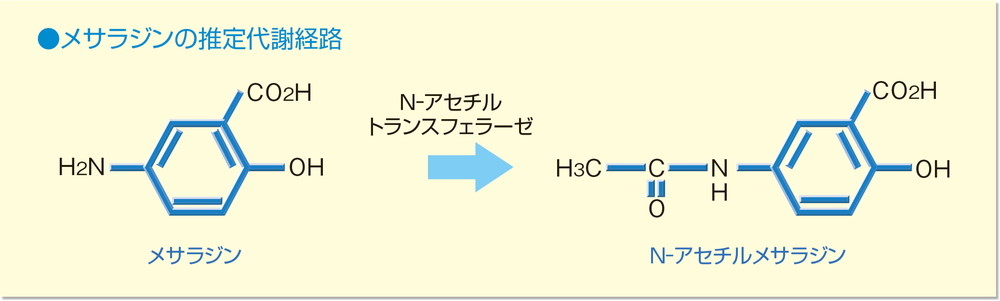
代謝(ヒト、ラット)3)
ヒトにおいて、メサラジンは全身に分布するN-アセチルトランスフェラーゼによって生体内で安定なアセチル体(N-アセチルメサラジン)に代謝されます。主な代謝部位は肝臓、消化管です。
メサラジンの主代謝物であるアセチル体はラット酢酸誘発大腸炎モデルに対して作用を示さず(in vivo)、フリーラジカル還元作用、過酸化水素消去作用、次亜塩素酸イオン消去作用、過酸化脂質抑制作用及びスーパーオキサイド消去作用は認められませんでした。LTB4生合成に対しては1×10-3Mで抑制率が54.2%でした(in vitro)。
以上の結果から、アセチル体には薬理作用は認められないと推察されました。
排泄1) <外国人データ>
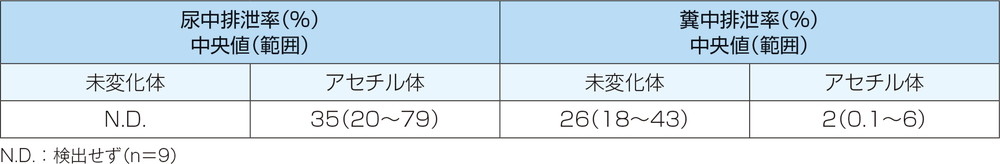
潰瘍性大腸炎患者9例にメサラジン注腸剤100mL(メサラジンとして1g含有)を単回経直腸投与したときの投与後48時間までの排泄率は、尿中では未変化体は検出せず、アセチル体が35%(中央値、範囲20~79%)であり、糞中では未変化体が26%(中央値、範囲18~43%)、アセチル体が2%(中央値、範囲0.1~6%)でした。
【メサラジン注腸剤(1g/100mL、pH4.8)を単回投与したときの投与後48時間までの尿及び糞中排泄率】
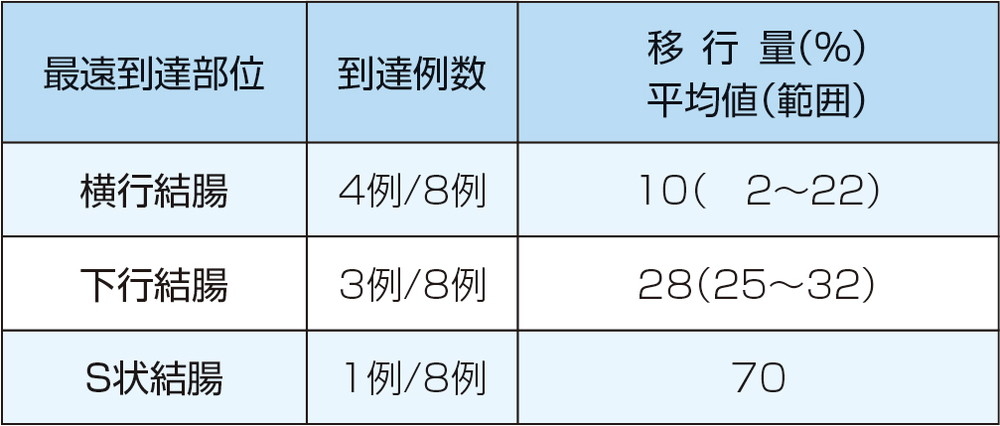
その他4)<外国人データ>
健康成人8例にメサラジン(99mTc標識体)注腸剤(1g/100mL)を経直腸投与し、腸内での最遠到達部位と移行量を投与後4時間まで測定しました。なお、薬剤は被験者を左側臥位にして投与し、薬剤保持のため2時間そのままの体位を維持しました。その結果、7例が脾彎曲部まで到達し、このうち4例は横行結腸まで到達しました。
- 1) Bondesen S. et al:Scand J Gastroenterol 1984;19:677-682
- 2) 海外反復投与試験(社内資料)
- 3) 中丸幸一 他:日薬理誌 1994;104:447-457
- 4) Brown J. et al:Alimental Pharmacol Ther 1997;11:685-691
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

