-薬効薬理-
QT/QTc間隔延長に対する作用1)[経口投与試験]
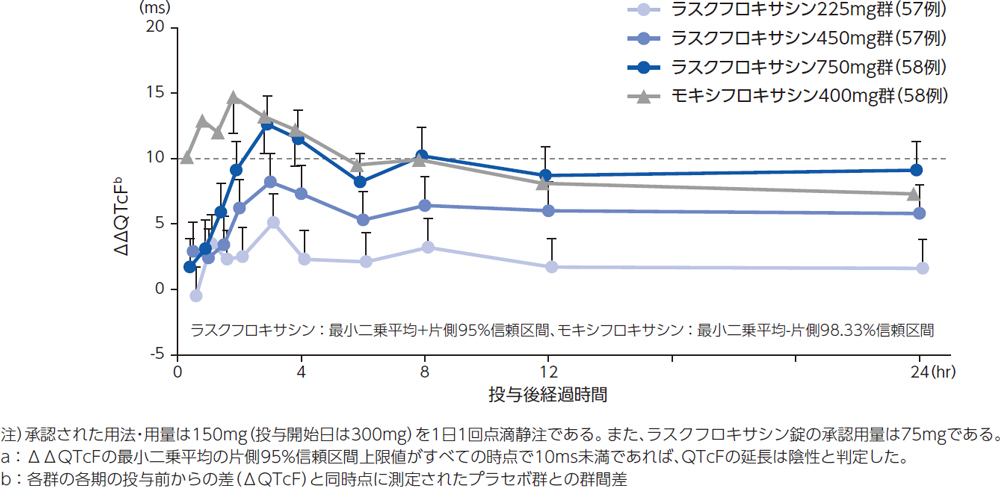
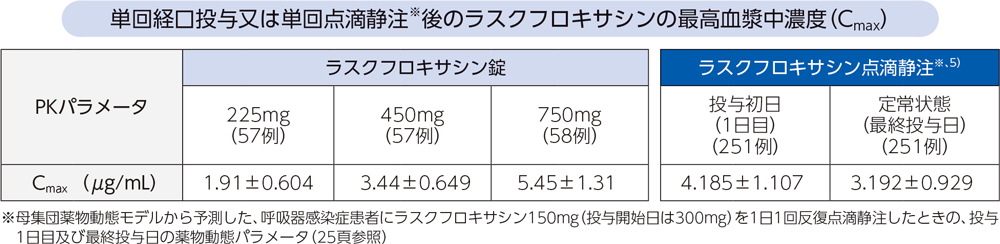
健康成人のべ172例を対象とした無作為化二重盲検クロスオーバー試験において、ラスクフロキサシン225mg注)(57例)、450mg注)(57例)及び750mg注)(58例)単回経口投与時のQT/QTc延長をQTcF(Fridericia法による心拍数補正QT)を用いて評価した結果、225mg投与群が陰性、450mg投与群以上で陽性と判定されたa。なお、健康成人に450mg経口投与時のCmax(3.44±0.649μg/mL)は、呼吸器感染症患者に本剤の用法・用量投与時のCmax(投与初日4.185±1.107μg/mL、定常状態3.192±0.929μg/mL)2)と同程度である。
2. 禁忌(次の患者には投与しないこと)〈抜粋〉
- 2.2
- QT延長のある患者(先天性QT延長症候群等)[8.3、9.1.2、11.1.4参照]
- 2.3
- 低カリウム血症のある患者[9.1.2、11.1.4参照]
- 2.4
- クラスⅠA(キニジン、プロカインアミド等)又はクラスⅢ(アミオダロン、ソタロール等)の抗不整脈薬を投与中の患者[10.1参照]
- 2.5
- 重度の肝機能障害のある患者[9.3.1参照]
- 8.
- 重要な基本的注意〈抜粋〉
- 8.3
- 本剤投与によりQT間隔が延長するおそれがあるため、本剤の投与開始前及び投与中は患者の状態を十分に観察し、必要に応じて心電図検査等を実施すること。[2.2、9.1.2、11.1.4参照]
- 9.
- 特定の背景を有する患者に関する注意〈抜粋〉
- 9.1
- 合併症・既往歴等のある患者
- 9.1.2
- 重度の徐脈等の不整脈、虚血性心疾患、心不全等の心疾患のある患者
心室頻拍(Torsade de pointesを含む)、QT延長を起こすおそれがある。[2.2、2.3、8.3、11.1.4参照]
- 9.3
- 肝機能障害患者
- 9.3.1
- 重度の肝機能障害のある患者
投与しないこと。血漿中濃度上昇のおそれがある。[2.5参照]
- 10
- 相互作用〈抜粋〉
- 10.1
- 併用禁忌(併用しないこと)
クラスⅠA抗不整脈薬 キニジン、プロカインアミド等
クラスⅢ抗不整脈薬 アミオダロン、ソタロール等[2.4参照]
- 11
- 副作用〈抜粋〉
- 11.1
- 重大な副作用
- 11.1.4
- QT延長、心室頻拍(Torsade de pointesを含む)(いずれも頻度不明)[2.2、2.3、8.3、9.1.2参照]
作用機序
(1)DNAジャイレース及びトポイソメレースⅣに対する阻害作用
ラスクフロキサシンは、細菌のDNAジャイレース及びトポイソメレースⅣを阻害し、殺菌的に作用する3)。
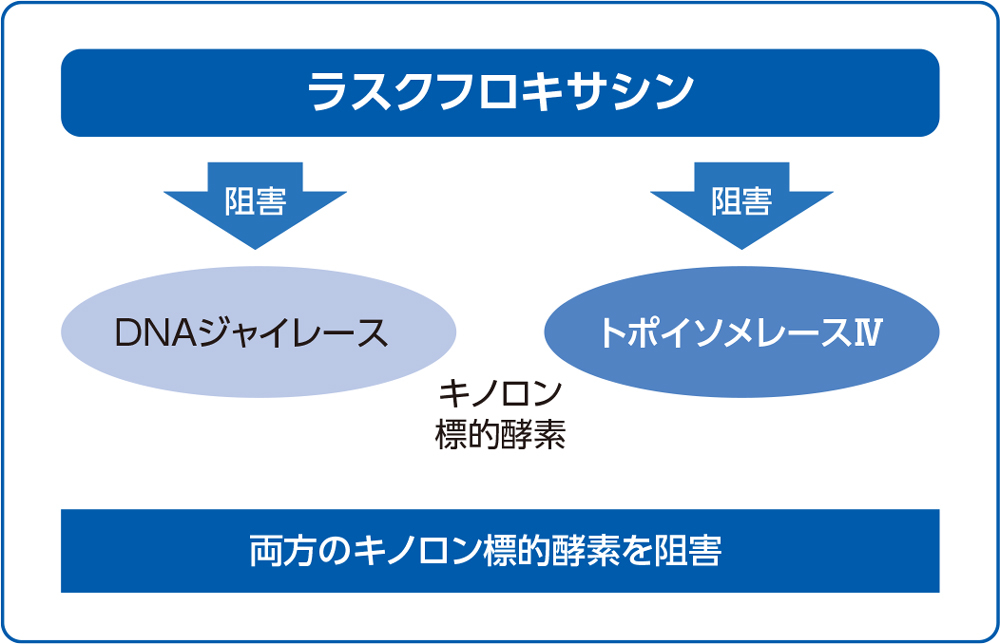
両方のキノロン標的酵素を阻害する薬剤は耐性菌を作りにくいことが示唆されている3〜6)。
非臨床試験
(1)キノロン標的酵素変異株に対する抗菌力(in vitro)7)
1)黄色ブドウ球菌
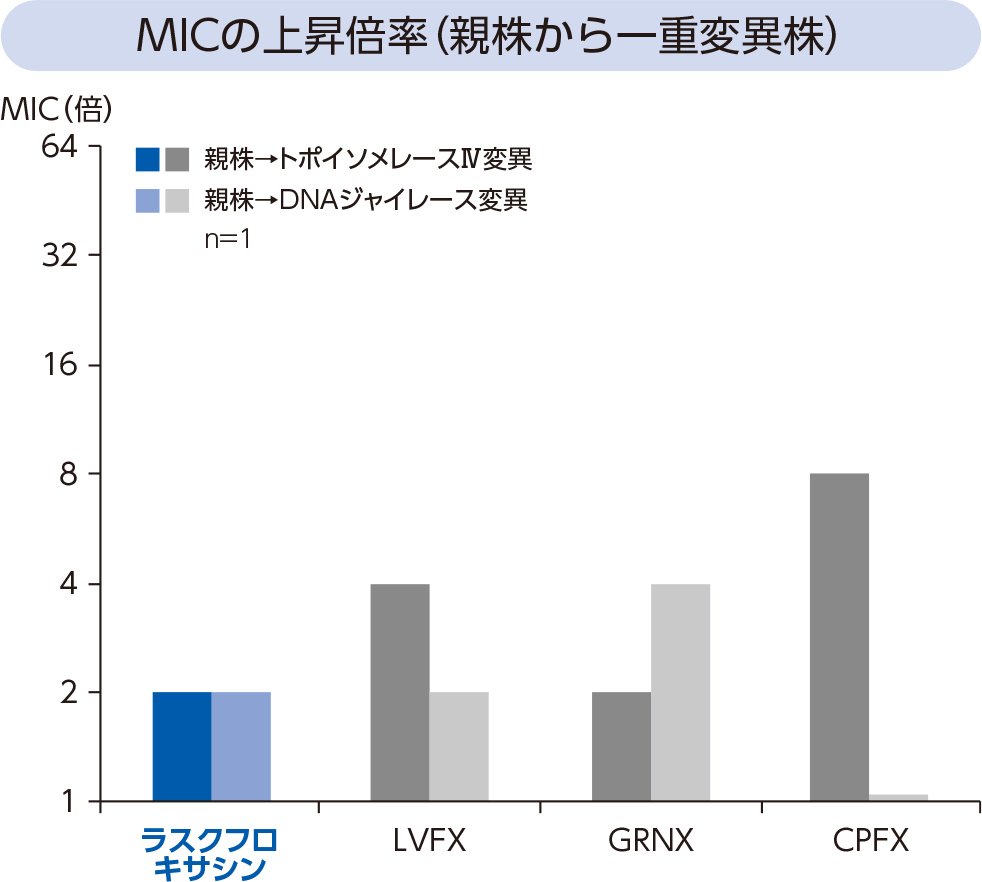
黄色ブドウ球菌の標的酵素変異株に対するラスクフロキサシンの抗菌力を測定した結果、DNAジャイレース又はトポイソメレースⅣの変異によるMIC上昇倍率は、親株から一重変異株ではいずれも2倍、一重変異株から二重変異株ではいずれも4倍であることから、ラスクフロキサシンは菌体内で両方のキノロン酵素を阻害する薬剤として働いていることが示唆された。さらに四重変異株に対するラスクフロキサシンのMICは2μg/mLであった。
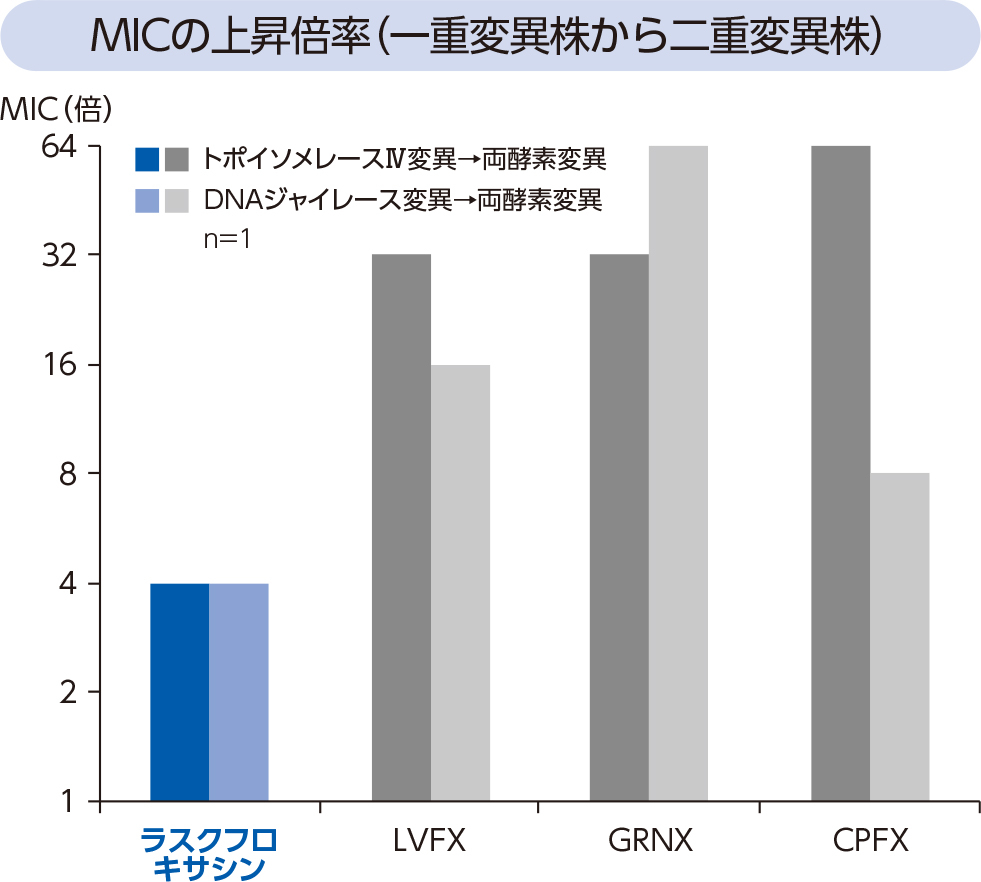
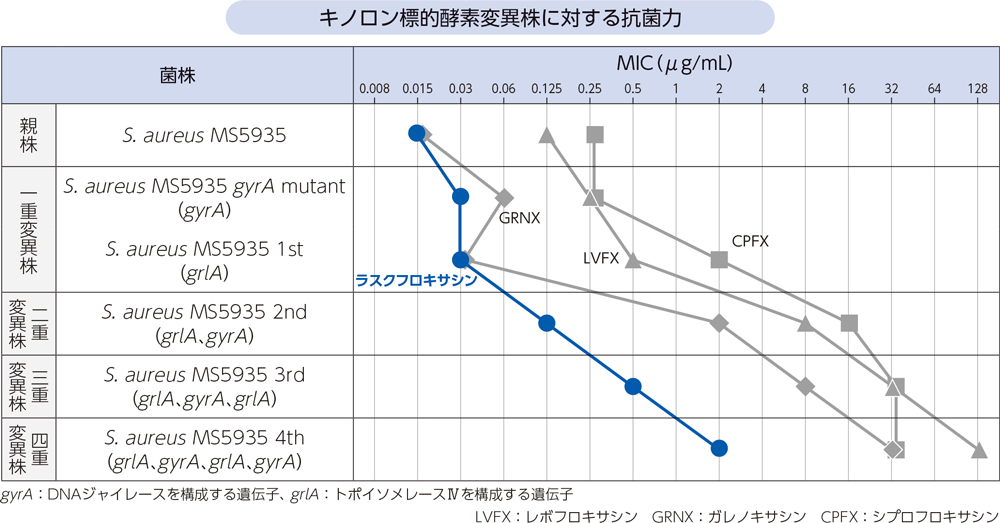
- [方法]
- 黄色ブドウ球菌(親株:S. aureus MS5935、一重変異株:gyrA変異株又はgrlA変異株、二重変異株:gyrA、grlA変異株)由来のDNAジャイレース及びトポイソメレースⅣに変異を有するキノロン標的酵素変異株に対するラスクフロキサシン及び類薬(LVFX、GRNX、CPFX)のMICをCLSI寒天平板希釈法に準拠して測定した。
2)肺炎球菌
ラスクフロキサシンは、肺炎球菌のDNAジャイレース変異及びトポイソメレースⅣ変異による抗菌力の低下の結果より、両方のキノロン酵素を阻害する薬剤であることが示唆された。
さらに二重変異株に対するラスクフロキサシンのMICは0.25〜0.5μg/mLであった。
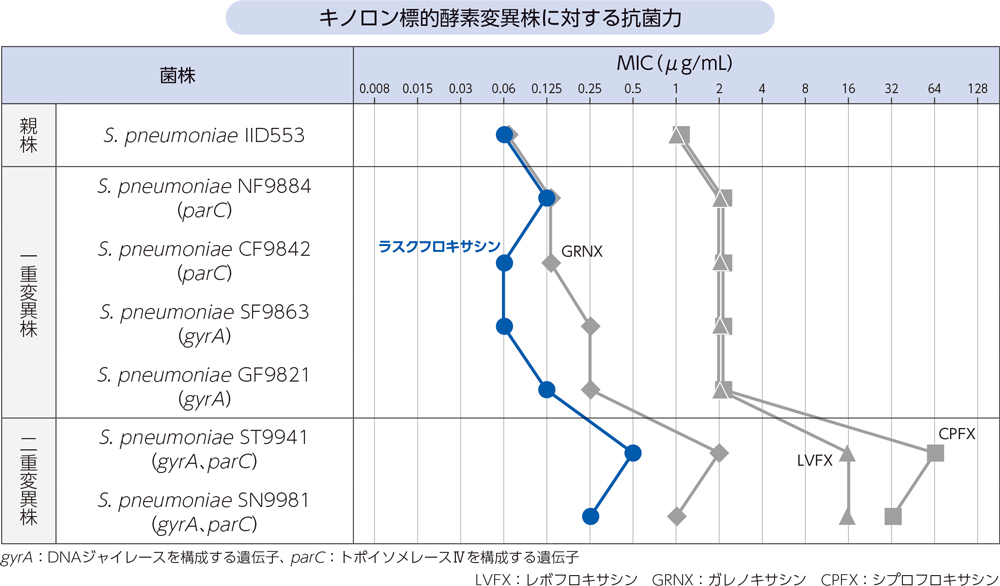
- [方法]
- 肺炎球菌(親株:S. pneumoniae IID553、一重変異株:gyrA変異株又はparC変異株、二重変異株:gyrA、parC変異株)由来のDNAジャイレース及びトポイソメレースⅣに変異を有するキノロン標的酵素変異株に対するラスクフロキサシン及び類薬(LVFX、GRNX、CPFX)のMICをCLSI微量液体希釈法に準拠して測定した。
(2)細菌とヒトのⅡ型トポイソメレースに対する選択性(in vitro)7)
ラスクフロキサシンのヒトトポイソメレースⅡに対する阻害活性(IC50)は>2,400μg/mL、細菌のⅡ型トポイソメレース(トポイソメレースⅣ及びDNAジャイレース)に対する阻害活性は6.0±0.2μg/mL以下であった。
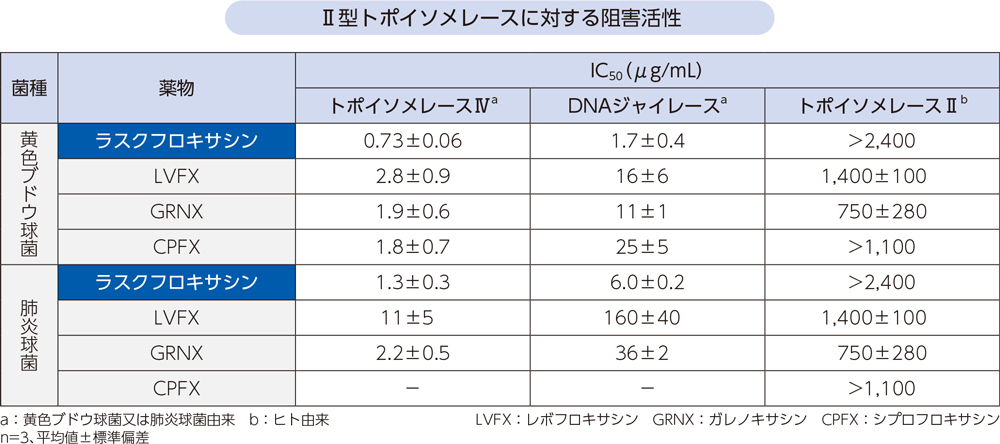
- [方法]
- 黄色ブドウ球菌又は肺炎球菌由来のトポイソメレースⅣ、DNAジャイレース、ヒト由来のトポイソメレースⅡに対するラスクフロキサシン及び類薬(LVFX、GRNX、CPFX)の阻害活性(IC50値)をそれぞれ測定した。
(3)抗菌力(in vitro)7)
1)標準株に対する抗菌スペクトル
ラスクフロキサシンはグラム陽性菌及び陰性菌、嫌気性菌、非定型菌に対して以下の抗菌力を示した。
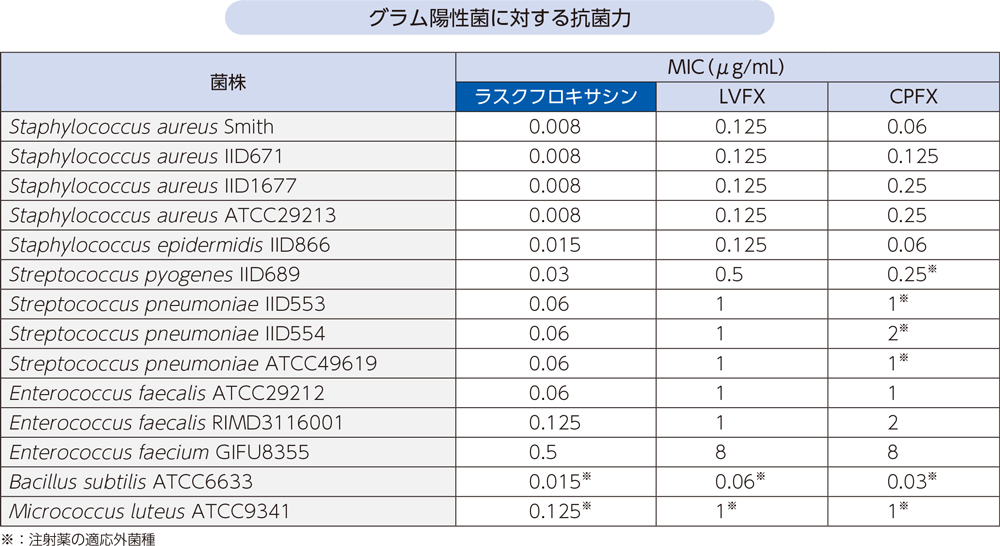
- [方法]
- グラム陽性菌の標準株に対するラスクフロキサシン及び類薬(LVFX、CPFX)のMICを測定した。S. pneumoniaeはCLSI微量液体希釈法、それ以外はCLSI寒天平板希釈法に準拠して測定した。
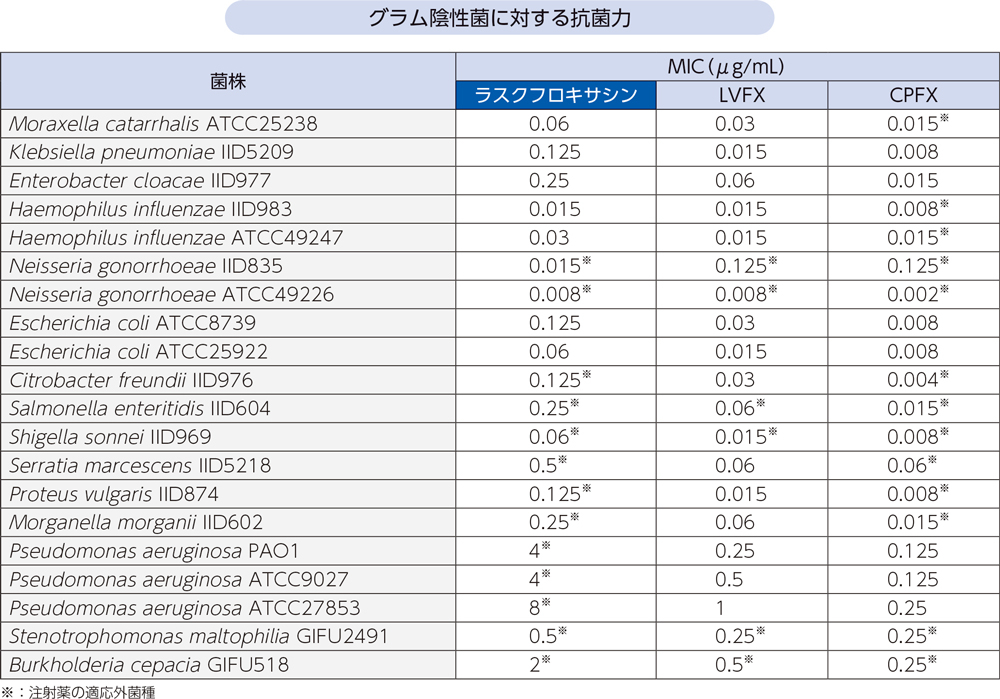
- [方法]
- グラム陰性菌の標準株に対するラスクフロキサシン及び類薬(LVFX、CPFX)のMICを測定した。H. influenzaeはCLSI微量液体希釈法、それ以外はCLSI寒天平板希釈法に準拠して測定した。
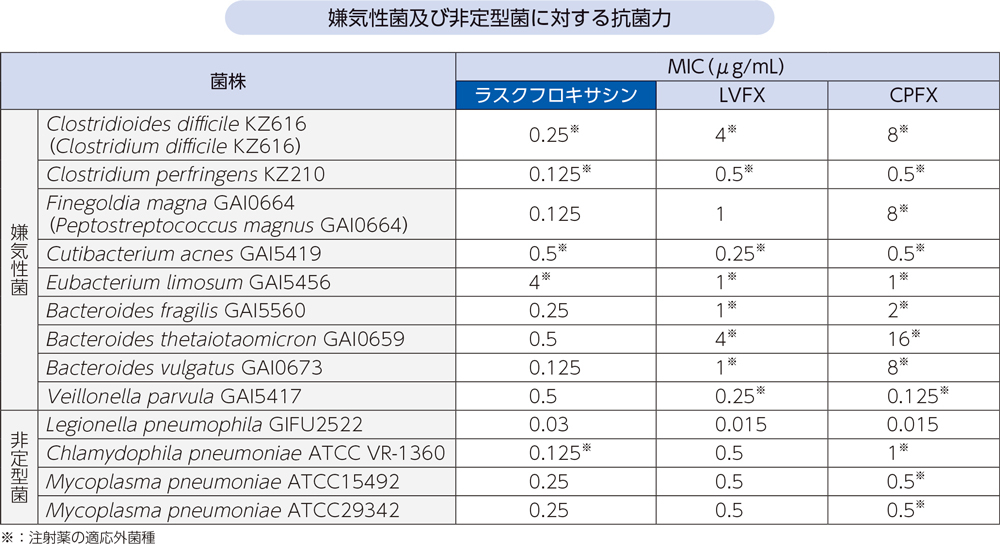
- [方法]
- 嫌気性菌及び非定型菌の標準株に対するラスクフロキサシン及び類薬(LVFX、CPFX)のMICを測定した。嫌気性菌はCLSI寒天平板希釈法、M. pneumoniaeに対しては尾形ら及びYamaguchiらの方法8、9)を一部改変した微量液体希釈法、L. pneumophilaは猿渡らの方法10)を一部改変した微量液体希釈法、C. pneumoniaeは日本化学療法学会標準法11)に準拠した方法で測定した。
2)臨床分離株に対する抗菌力[MIC90](in vitro)
ラスクフロキサシンはグラム陽性菌及び陰性菌、嫌気性菌、非定型菌に対し、以下の抗菌力を示した。

- [方法]
- 臨床分離株に対するラスクフロキサシン及び既存の抗菌薬(LVFX、AZM、CTRX、MEPM、PIPC/TAZ、CLDM、MNZ)のMIC90をCLSI微量液体希釈法に準拠して測定した。
(4)耐性菌出現頻度(in vitro)7)
ラスクフロキサシンの耐性菌出現頻度は、黄色ブドウ球菌で2.1×10-9未満、肺炎球菌で1.1×10-8未満であり、試験した濃度範囲において耐性菌は選択されなかった。
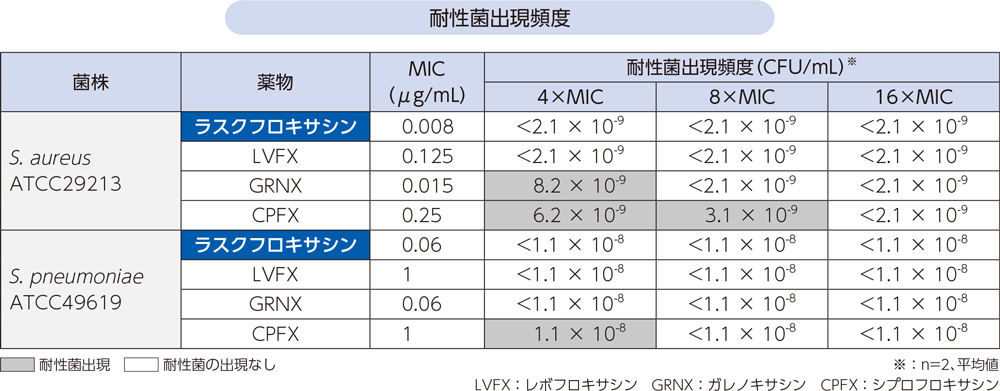
- [方法]
- 黄色ブドウ球菌又は肺炎球菌のラスクフロキサシンと類薬(LVFX、GRNX、CPFX)に対する耐性菌の出現頻度を測定した。各菌株に対するMICの4、8、16倍濃度の薬物存在下で約70時間培養したときの耐性菌出現頻度(CFU/mL)を測定し、平均値を算出した。
(5)耐性獲得試験(in vitro)7)
黄色ブドウ球菌及び肺炎球菌を7回継代培養したとき、ラスクフロキサシンのMIC上昇は継代前と比べ4倍であった。
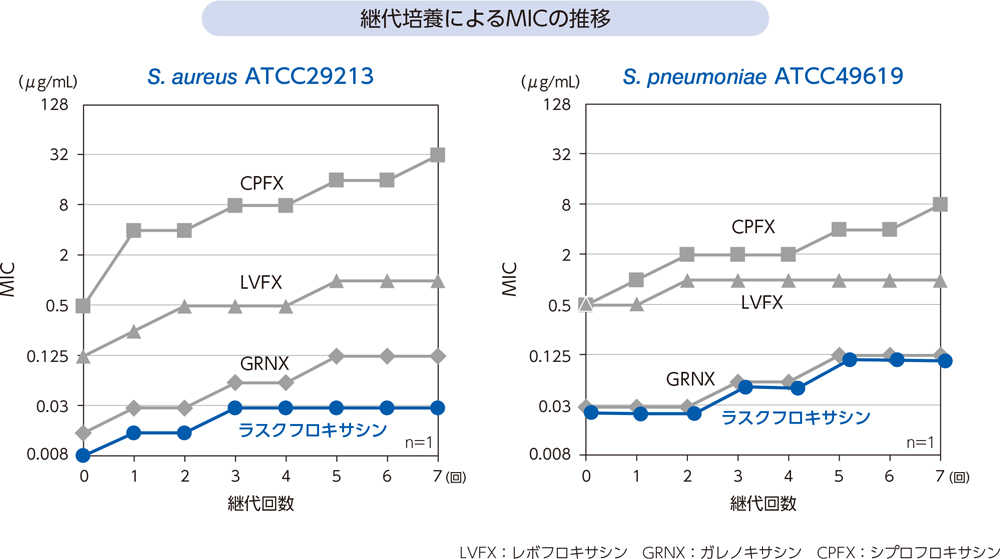
- [方法]
- 黄色ブドウ球菌又は肺炎球菌をラスクフロキサシン及び類薬(LVFX、GRNX、CPFX)含有液体培地中で培養して、MICを測定した後、目視にて菌株の発育が認められた濃度範囲における最高薬物濃度の培養液から菌株を継代培養し、再び薬物含有培地中で培養するという操作を7回繰り返し、この間のMICを測定した。
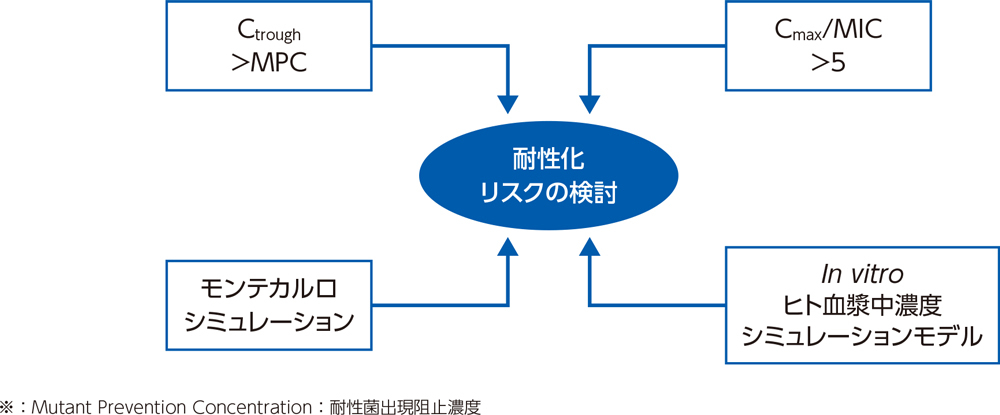
(6)耐性化リスクの検討
肺炎球菌においては、Cmax/MICが5未満の場合のみキノロン耐性菌が選択されたとの報告がある12)。また、MPCとMICの間の範囲はMSW(Mutant Selection Window:耐性菌選択域)と呼ばれ、MSWの範囲内では耐性菌を発現させる可能性が高くなることが報告されている13)。
これらをもとに、ラスビック®点滴静注キット150mg(初日は300mg)1日1回投与における肺炎球菌の耐性化リスクについて検討した。
1)Cmax/MIC14〜16)
ラスビック®点滴静注キット150mg(初日は300mg)を1日1回投与した呼吸器感染症患者で肺炎球菌が検出された32例全例において、Cmax/MICが5を上回った。またモンテカルロシミュレーションを用いた検討から、投与初日にCmax/MICが5を上回る確率は100%であった。
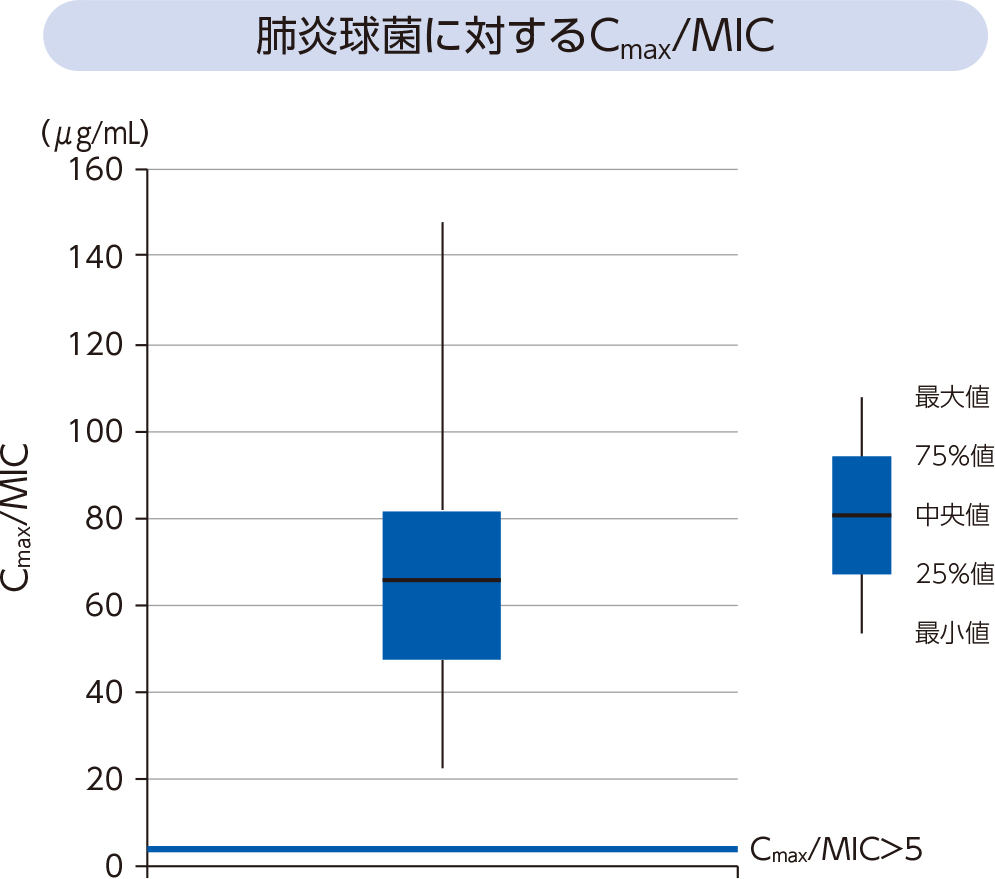

- [方法]
- ラスビック®点滴静注キット150mg(初日は300mg)を1日1回投与した呼吸器感染症患者で肺炎球菌が検出された32例におけるCmax/MICをPPKモデルで算出した。次にPPKモデルを用いて、呼吸器感染症患者10,000例を発生させたモンテカルロシミュレーションにより本剤を7日間反復点滴静注投与時の血漿中濃度推移を算出した。PPKモデルの共変量データは、呼吸器感染症の患者データと同様の分布となるように作成した。また、PPKパラメータの推定値と本剤の臨床試験で得られた肺炎球菌のMIC分布を用いて患者10,000例分のCmax/MIC仮想データを作成し、本剤投与時のCmax/MICが5を上回る確率を推定した。
2)Ctrough14〜16)
ラスビック®点滴静注キット150mg(初日は300mg)を1日1回投与した呼吸器感染症患者で肺炎球菌が検出された33例全例において、Ctroughが0.12μg/mLを上回った。またモンテカルロシミュレーションを用いた検討から、投与初日にCtroughが肺炎球菌のMPC 0.12μg/mLを上回る確率は100%であった。
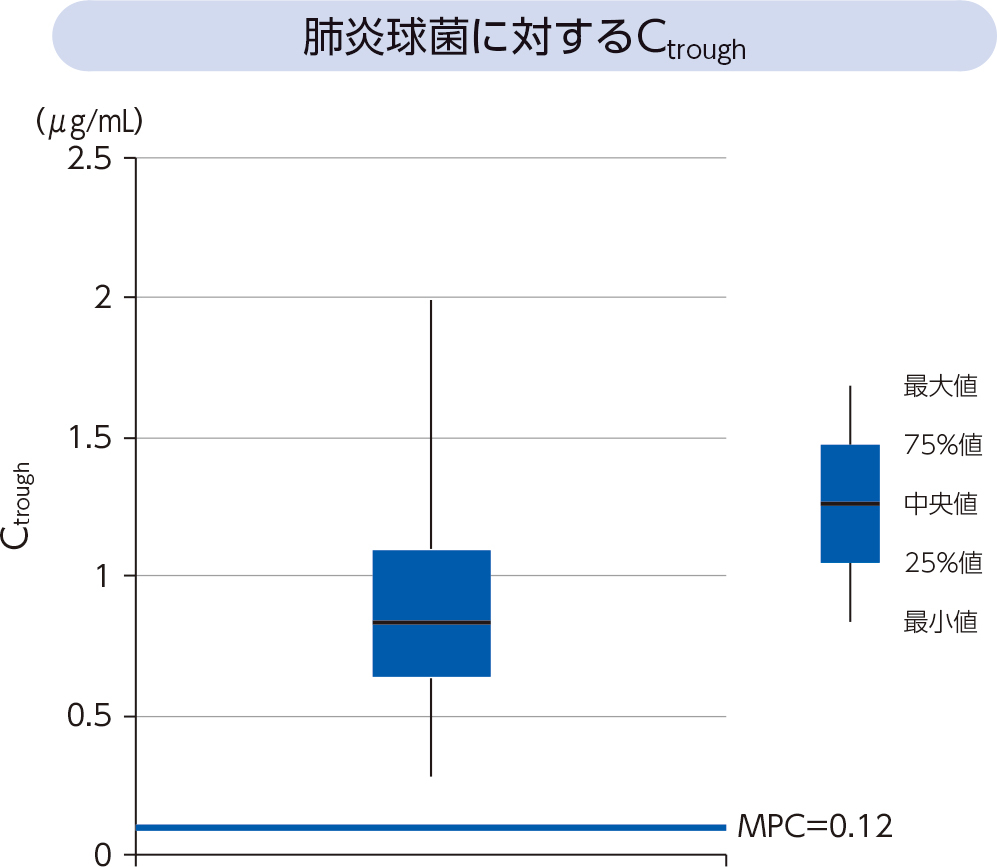
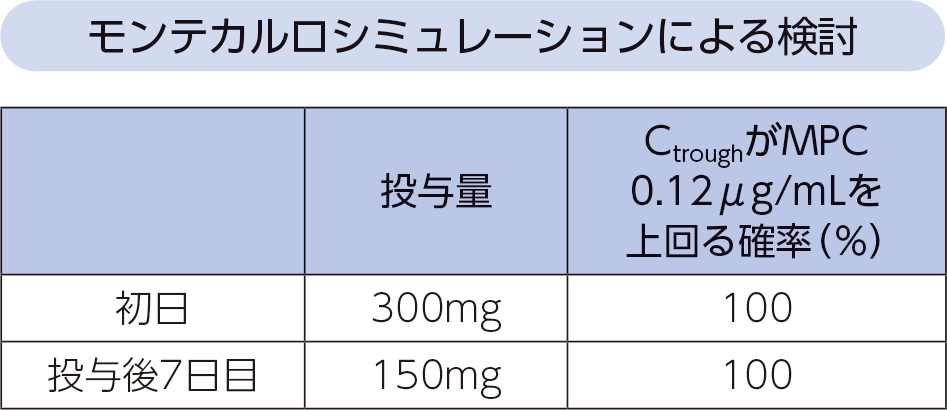
- [方法]
- ラスビック®点滴静注キット150mg(初日は300mg)を1日1回投与した呼吸器感染症患者で肺炎球菌が検出された33例におけるCtroughをPPKモデルで算出した。またCtroughが非臨床試験で確認した肺炎球菌に対するMPC 0.12μg/mLを上回る患者の割合を評価した。次にPPKモデルを用いて、呼吸器感染症患者10,000例を発生させたモンテカルロシミュレーションにより本剤を7日間反復点滴静注投与時の血漿中濃度推移を算出した。PPKモデルの共変量データは、呼吸器感染症の患者データと同様の分布となるように作成した。本剤投与時のCtroughが非臨床試験で確認した肺炎球菌に対するMPC 0.12μg/mLを上回る確率を推定した。
3)ヒト血漿中濃度シミュレーションモデルにおける肺炎球菌に対する殺菌作用(in vitro)7)
ラスクフロキサシンは、肺炎球菌の野生株及びキノロン標的酵素変異株に対し、シミュレーション開始6時間後までに検出限界以下に殺菌し、24時間後に再増殖した株は認められなかった。
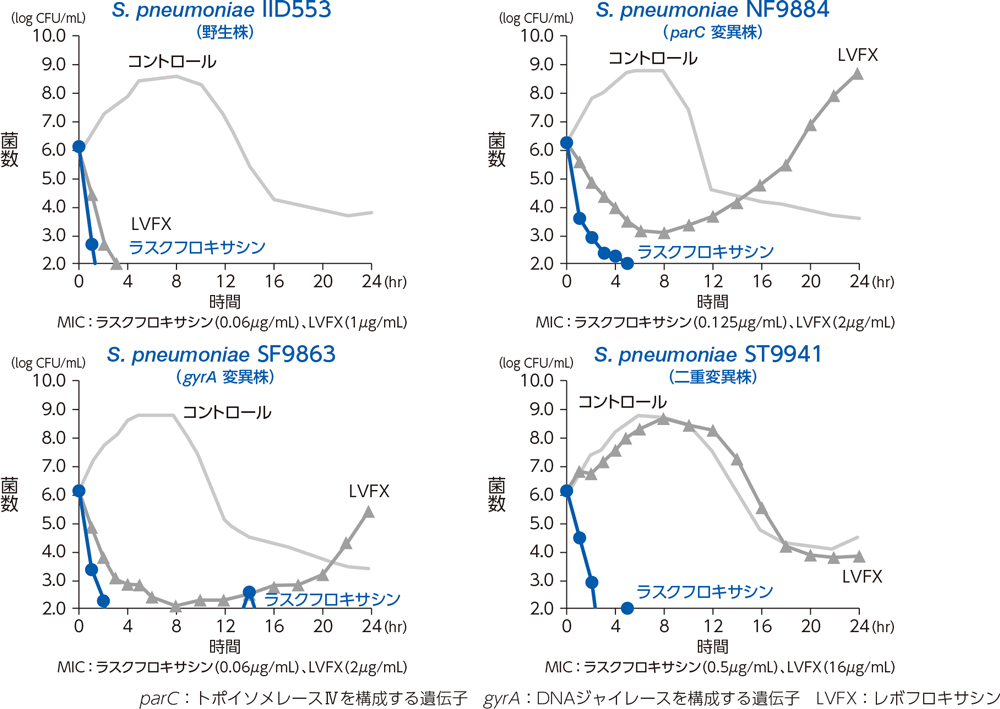
- [方法]
- ヒト血漿中濃度シミュレーションモデルを用いて、肺炎球菌に対するラスクフロキサシン300mgとLVFX500mgの単回静脈内投与時の殺菌効果を検討した。
- 1)承認時評価資料:ラスクフロキサシン(錠)の臨床薬理試験.
- 2)承認時評価資料:ラスクフロキサシン(点滴静注)の臨床薬理試験.
-
3)Kishii R, et al., Antimicrob. Agents Chemother. 61(6): e00120-17(2017)
利益相反:本論文の著者全員が杏林製薬株式会社の社員である。 -
4)Fukuda H, et al., Antimicrob. Agents Chemother. 42: 1917-1922(1998)
利益相反:本論文の著者全員が杏林製薬株式会社の社員である。 -
5)Takei M, et al., Antimicrob. Agents Chemother. 45: 3544-3547(2001)
利益相反:本論文の著者全員が杏林製薬株式会社の社員である。 -
6)Fukuda H, et al., Antimicrob. Agents Chemother. 45: 1649-1653(2001)
利益相反:本論文の著者全員が杏林製薬株式会社の社員である。 - 7)承認時評価資料:ラスクフロキサシンの薬効薬理試験.
- 8)尾形 学 監修, マイコプラズマとその実験法.近代出版, 441-448(1988)
- 9)Yamaguchi T, et al., Antimicrob. Agents Chemother. 44: 1381-1382(2000)
- 10)猿渡 克比孔 ほか, Legionellaに対する新しい薬剤感受性用培地(B-SYE 寒天培地)について.日本化学療法学会雑誌, 32:718-723(1984)
- 11)熊本悦明 ほか, クラミジアMIC測定法-日本化学療法学会標準法-(1991年改訂版).日本化学療法学会雑誌, 40: 303-307(1992)
- 12)Madaras-Kelly KJ, et al., Diagn Microbiol Infect Dis. 37(4): 253-260(2000)
- 13)戸塚恭一 三鴨廣繁 監修, 日常診療に役立つ抗感染症薬のPK-PD. ユニオンエース(2010)
- 14)承認時評価資料:市中肺炎患者を対象とした国内第Ⅲ相二重盲検比較試験(AMY-I301)
- 15)承認時評価資料:呼吸器感染症患者を対象とした国内第Ⅲ相非盲検非対照試験(AMY-I302)
- 16)承認時評価資料:市中肺炎を対象とした第Ⅱ相試験(用量設定試験)(AMY-I201)
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

