-国内第III相比較試験(プラセボ対照二重盲検比較試験)-
紹介する結果には承認用量と異なる成績が含まれていますが、承認審査過程で評価された試験成績であるため掲載しています。
イミダフェナシンは参照群です。本結果は参照群とベオーバとの比較を示したものではありません。
100mgは承認外の用量のため有効性に関する結果はベオーバ50mg群の結果のみ記載
社内資料:国内第Ⅲ相比較試験(T301試験)[承認時評価資料]
試験概要
| 目的 | 過活動膀胱(OAB)患者を対象にベオーバを12週間経口投与した際の有効性(プラセボ投与に対する優越性)及び安全性を検討する。 |
|---|---|
| 対象 | 20歳以上のOAB患者1,232例(有効性解析対象例1,224例、安全性解析対象例1,225例) |
| 方法 |
多施設共同無作為化二重盲検プラセボ対照並行群間比較試験 2週間の観察期(プラセボ投与、単盲検下)終了後に、患者をベオーバ50及び100mg群、参照薬(イミダフェナシン0.2mg)群又はプラセボ群に3.3 : 3.3 : 1 : 3.3の比で無作為に割り付け、12週間経口投与(1日1回朝食後)した。 |
| 主要評価項目 | 12週時の1日平均排尿回数のベースラインからの変化量 |
| 副次評価項目 |
・各評価時点におけるベースラインからの変化量 (①1日平均排尿回数、②1日平均尿意切迫感回数、③1日平均切迫性尿失禁回数、④1日平均尿失禁回数、⑤夜間平均排尿回数、⑥平均1回排尿量、⑦キング健康調査票によるquality of life(QOL)のドメインスコア)評価時点:①〜⑥4、8、12週、⑦試験終了時 ・Patient global impression(PGI)による自覚的改善度の有効改善、著効改善の割合 評価時点:試験終了時 |
| 安全性評価項目 | 有害事象、臨床検査、バイタルサイン、12誘導心電図検査、残尿量 |
| 解析計画 |
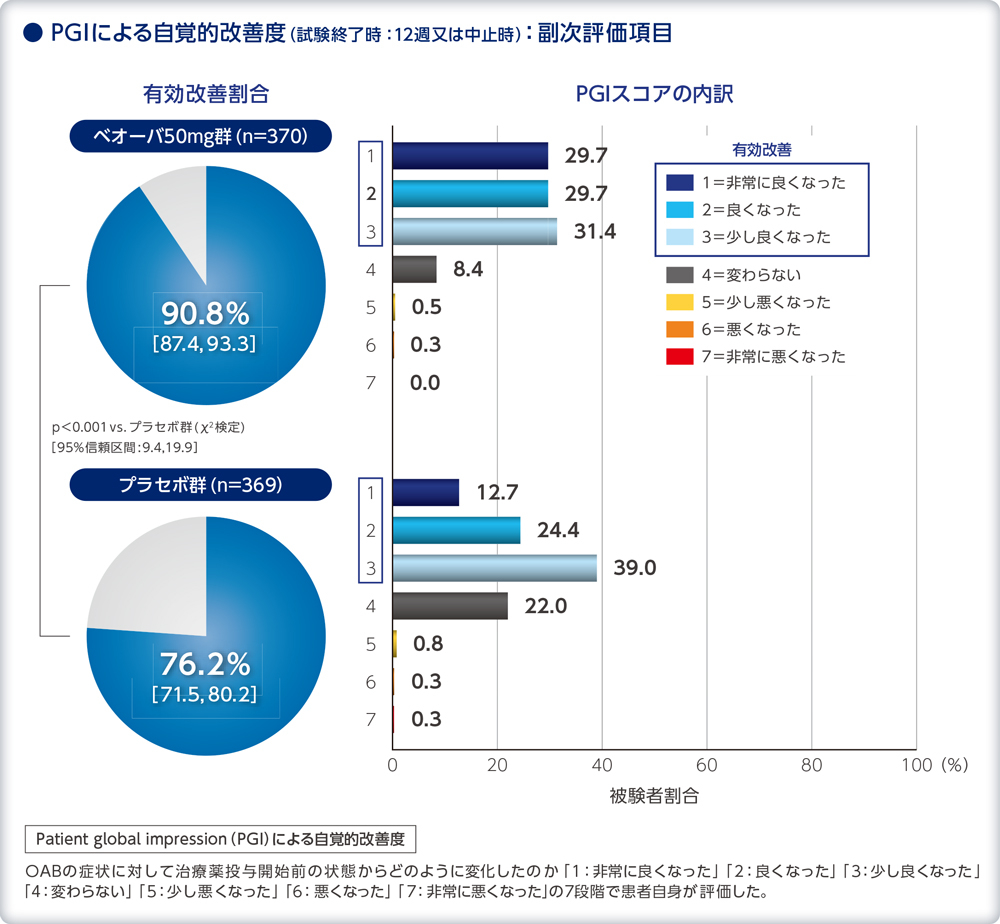
主要評価項目について、ベオーバ50mg及び100mg群のプラセボに対する優越性を、閉手順により多重性を考慮し、固定順検定方法を用いてベオーバ100mg群とプラセボ群の検定を行い、有意であった場合は50mg群とプラセボ群の検定を実施し、有意でない場合は検定を中止した(いずれも有意水準両側5%)。時点(週)、性別、OAB前治療歴、切迫性尿失禁の有無及び時点(週)と投与群の交互作用を含めた制約付き経時測定データ解析(cLDA法)を用いた群間比較により検証した。副次評価項目は、cLDA法あるいはX2検定を用いた。 PGIによる自覚的改善度の有効改善割合もしくは著効改善割合の算出及びその両側95%信頼区間を推定し、ベオーバ50mg群及び100mg群のプラセボ群に対する群間比較を実施した。群間比較はX2検定及び割合の群間差の両側95%信頼区間(Wald信頼区間)を推定した。 PGI による自覚的改善度の定義は以下のとおりとした。 (1)有効改善:PGI スコアが「1:非常に良くなった」、「2:良くなった」及び「3:少し良くなった」に該当。 (2)著効改善:PGI スコアが「1:非常に良くなった」及び「2:良くなった」に該当。 |
排尿パラメータのベースラインからの変化量(12週時)
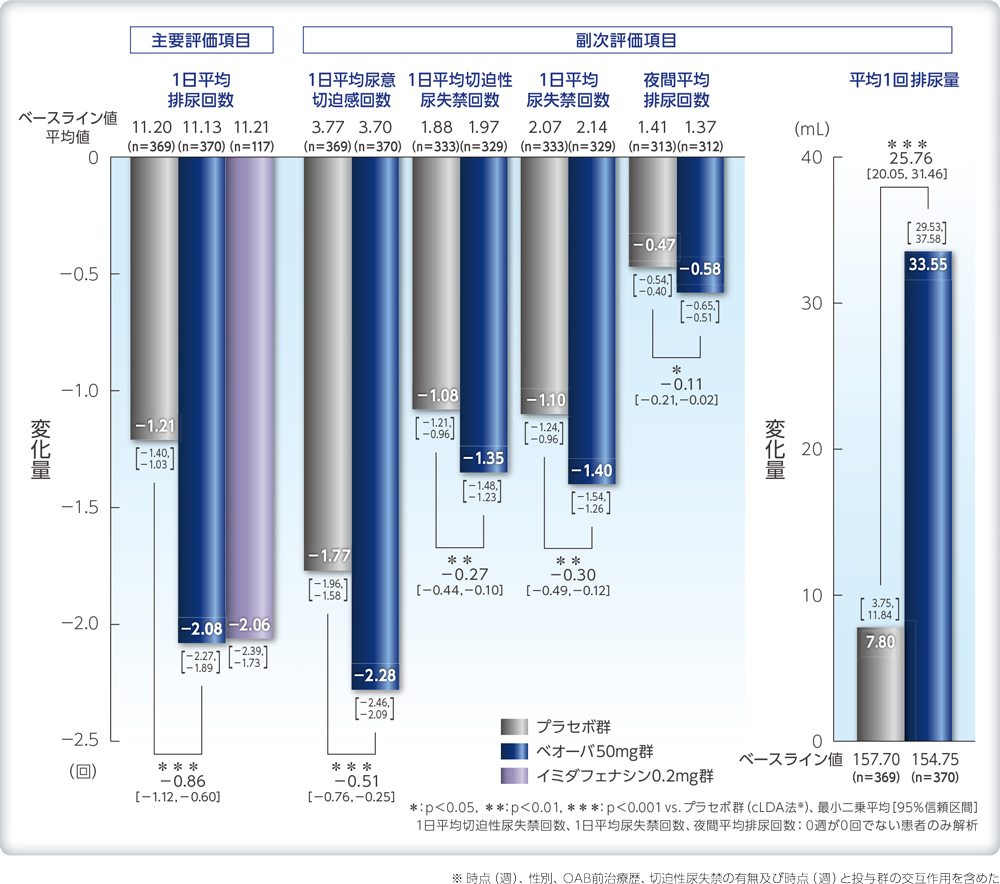
本剤の承認された用法及び用量は「通常、成人にはビベグロンとして50mgを1日1回食後に経口投与する。」である。
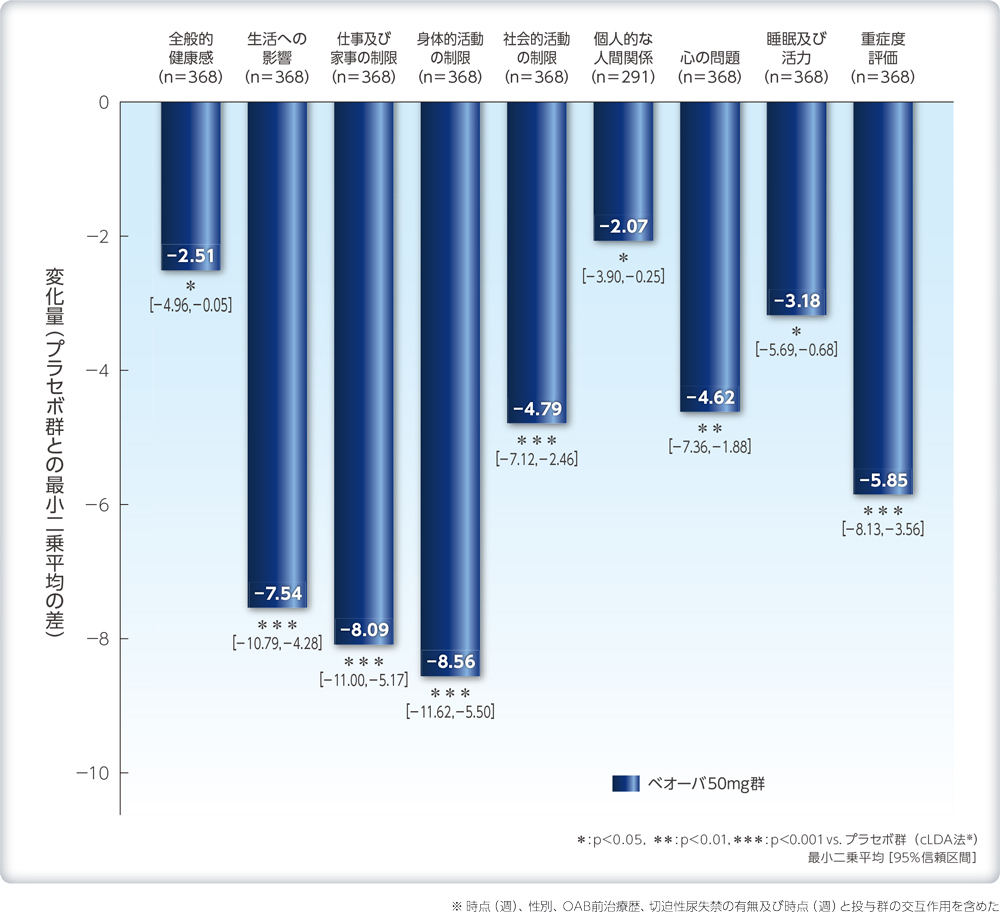
キング健康調査票によるQOLのドメインスコアのベースラインからの変化量のプラセボ群との差(試験終了時:12週又は中止時)副次評価項目
PGIによる自覚的改善度(試験終了時:12週又は中止時)副次評価項目
安全性(安全性解析対象例1,225例)
●副作用発現率
| プラセボ群 (n=369) |
ベオーバ50mg群 (n=370) |
ベオーバ100mg群 (n=369) |
イミダフェナシン0.2mg群 (n=117) |
|---|---|---|---|
| 19 (5.1) | 28 (7.6) | 20 (5.4) | 12 (10.3) |
例数(%)
●主な副作用(発現率1%以上)*
*いずれかの投与群で 1% 以上
| プラセボ群 (n=369) |
ベオーバ50mg群 (n=370) |
ベオーバ100mg群 (n=369) |
イミダフェナシン0.2mg群 (n=117) |
|
|---|---|---|---|---|
| 便秘 | 3 (0.8) | 6 (1.6) | 1 (0.3) | 1 (0.9) |
| 口内乾燥 | 2 (0.5) | 5 (1.4) | 1 (0.3) | 5 (4.3) |
| 血中アルカリホスファターゼ増加 | 1 (0.3) | - | 1 (0.3) | 2 (1.7) |
| 高血圧 | - | - | - | 2 (1.7) |
例数(%)
●投与中止に至った副作用
| プラセボ群 (n=369) |
ベオーバ50mg群 (n=370) |
ベオーバ100mg群 (n=369) |
イミダフェナシン0.2mg群 (n=117) |
|---|---|---|---|
| 1例1件 | 3例3件 | 2例3件 | 1例1件 |
| 上腹部痛 | 浮腫、好中球数減少、湿疹 | 傾眠、血中クレアチニン増加及び肝機能異常 | 高血圧 |
本試験において死亡例、重篤な副作用はいずれの投与群でも認められなかった。
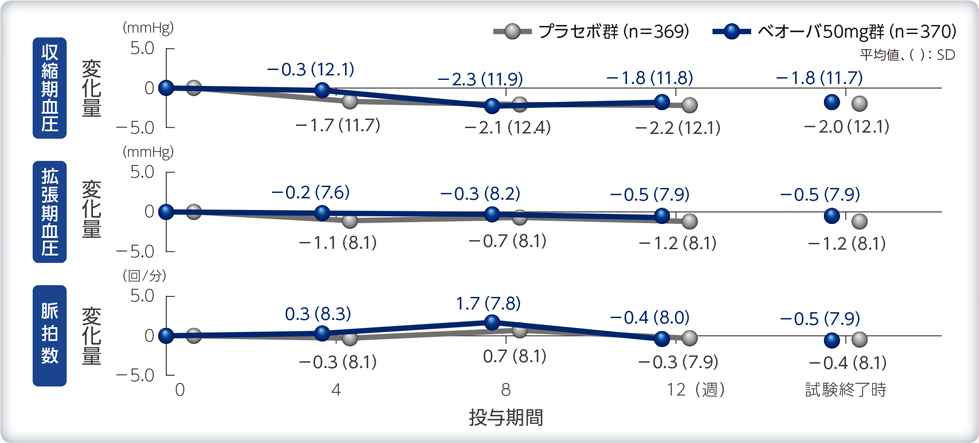
バイタルサインへの影響
バイタルサインのベースラインからの変化量の推移
9. 特定の背景を有する患者に関する注意(電子添文抜粋)
9.1 合併症・既往歴等のある患者
9.1.1 重篤な心疾患のある患者
心拍数増加等により、症状が悪化するおそれがある。
本剤の承認された用法及び用量は「通常、成人にはビベグロンとして 50mg を1日1回食後に経口投与する。」である。
禁忌を含む注意事項等情報につきましては電子添文をご参照ください。

